ゾサノファーマ社とのライセンス契約も解約
旭化成ファーマ株式会社と、米Zosano Pharma, Inc. (以下、ゾサノファーマ社)は、1月31日、ゾサノファーマ社が開発した経皮的微小突起薬物送達システムを活かしたヒト副甲状腺ホルモン(ヒトPTH)「テリボン」の経皮吸収製剤に関し、日本国内における開発を中止することを決定したと発表した。開発中止ととともに、両社で締結していたライセンス契約も解約したという。
旭化成ファーマはゾサノファーマ社と、2011年2月に日本における独占的開発・製造・販売権を旭化成ファーマが取得することを定めたライセンス契約を結んでいた。同年10月には、ヒトPTH製剤の骨粗鬆症治療薬「テリボン」において、ゾサノファーマ社のもつ技術を活かした微小突起型パッチ製剤タイプを新投与経路製剤として開発、臨床試験の準備が整ったことを発表していた。
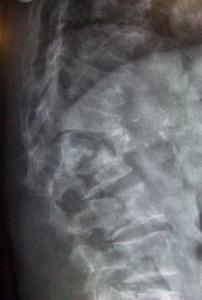
(画像はwikiメディアより引用)
第1相臨床試験で第2相臨床試験への移行基準を満たさず、開発中止に
ゾサノファーマ社の経皮的微小突起薬物送達システムは、治療薬物を多数の微小突起を介し、皮膚表皮に浸透させるという、迅速で効率的な薬物送達のシステム。さまざまな医療用ペプチドやタンパク質、低分子およびワクチンを、自己投与可能なニードルフリーなものとすることができるため、針とシリンジを用いる注射製剤に対し、簡便性の点で大きなメリットを有すると考えられている。このシステムを利用した経皮製剤は、薬物が被覆された微小突起の配置されている薄膜が装着された粘着性パッチと、再利用可能なアプリケータからなる。
ヒトPTH製剤である「テリボン」は、2011年11月25日に旭化成ファーマから「テリボン皮下注用56.5μg」(一般名:テリパラチド酢酸塩)として、骨折の危険性の高い骨粗鬆症を効能・効果とし発売された。通常成人に1週間に1回皮下注射するもので、投与は72週間までとされている。
骨形成促進作用を有し、国内で実施した第3相臨床試験では、週1回72週間の皮下投与でプラセボ群に比べ、新規椎体骨折の発生リスクを78.6%減少させたことが確認されている。骨折抑制効果は、骨の質を改善しながら、骨量を増やすことによって骨の強度が向上することでもたらされるものであり、社会的にも重要な課題とされる骨粗鬆症対策・骨粗鬆症治療に貢献する薬剤とみなされている。
今回の発表によると、開発中であった「テリボン」の経皮吸収製剤は、実施された第1相臨床試験において、旭化成ファーマが定めた第2臨床試験への移行基準を満たさなかったという。具体的なデータ等は公表されていないが、この臨床試験結果から、開発中止を決定するに至ったとされている。
なお旭化成ファーマでは、この経皮吸収製剤については開発を中止したものの、今後も「テリボン」に関して、さらに有用性の高い製剤の開発に取り組んでいく方針であるとしている。(紫音 裕)
▼外部リンク
旭化成ファーマ株式会社 プレスリリース
http://www.asahi-kasei.co.jp/asahi/jp/news/
Zosano Pharma, Inc.
http://www.zosanopharma.com/




