東京都医学研究所と共同研究
東北大学大学院医学研究科医化学分野の山本雅之教授らは、公益財団法人東京都医学総合研究所との共同研究で、二つの生体防御機構の連動と、このしくみをがん細胞がその増殖に利用していることを明らかにしたと発表した。
(画像はプレスリリースより)
この研究は、米国科学雑誌「MOLECULAR CELL」オンライン版に掲載されている。
オートファジーとKeap1-Nrf2経路がp62で連動
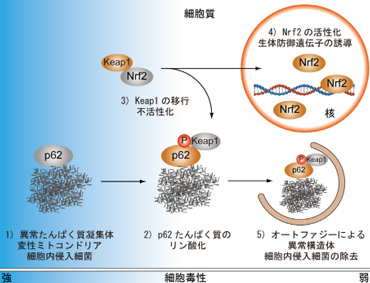
研究では、細胞内の消化分解機構であるオートファジーと、細胞のストレスセンサーによる防護システムであるKeap1-Nrf2経路が、ストレスに反応するタンパク質p62のリン酸化を介して連動していることを明らかにした。
オートファジーは、細胞質に出現した構造体が細胞質成分を取り囲んでオートファゴソームを形成し、これがリソソームと融合して内容物を消化する。この機構は、機能を失った異常ミトコンドリアや、細胞内に侵入した細菌を排除し、細胞の恒常性を保っている。
一方、Keap1-Nrf2経路は、細胞のストレスにセンサーとしてKeap1が働き、Keap1の不活性化によって転写因子Nrf2が活性化され、抗酸化タンパク質や抗炎症性酵素の遺伝子を誘導して細胞を守る。
p62はストレスによって細胞内に生じた異常タンパクの凝集体などをオートファゴソームに輸送する受容体だと考えられてきたが、研究チームによって、p62が異常タンパク質や細菌等に集積してリン酸化され、その結果p62とKeap1の結合が著しく増強されること、その結果Nrf2の活性化が促進されることを見出した。
肝細胞がんでp62のリン酸化が亢進
肝細胞がんの細胞株や患者組織などにおいては、恒常的にp62がリン酸化、Nrf2が活性化されており、研究では、p62のリン酸化を抑制すると、がん細胞の増殖が著しく抑制されることも確認。細胞の生体防御機構を使って、がん細胞が増殖していることが示唆されている。
これらの結果から、今後p62のリン酸化やKeap1との結合を標的として、新しい肝細胞がん治療薬が生まれる可能性がある。研究グループでは、現在創薬オープンイノベーションセンター保有の化合物を用いて化合物のスクリーニングを行っている。(長澤 直)
▼外部リンク
東北大学プレスリリース
http://www.tohoku.ac.jp/




