選択的IDO1酵素阻害剤「epacadostat」とキイトルーダの併用療法
米Merck & Co., Inc., Kenilworth, N.J., U.S.A.は6月5日、米Incyte社の選択的IDO1酵素阻害剤「epacadostat」(INCB024360)と、抗PD-1抗体「キイトルーダ(R)」(一般名:ペムブロリズマブ)との併用療法を検討する進行中の第1/2相臨床試験「ECHO-202」(KEYNOTE-037)の最新データを発表した。この結果は、2017年米国臨床腫瘍学会(ASCO)年次総会で複数発表された。
画像はリリースより
epacadostatは、Incyte社が開発中の経口投与可能な強力な選択的インドールアミン2,3-ジオキシゲナーゼ 1(IDO1)酵素阻害剤。がん免疫微小環境を制御することによって、がんに対する効果的な免疫反応を回復させる。単群試験では、切除不能または転移性悪性黒色腫患者に対して、同剤と免疫チェックポイント阻害剤との併用療法という概念実証が示されていた。これらの試験では、免疫チェックポイント阻害剤単独療法と比較して、同剤と抗CTLA-4抗体イピリムマブまたは抗PD-1抗体キイトルーダとの併用療法により奏効率が向上したという。
ECHO-202試験は、epacadostatをキイトルーダと併用投与したときの安全性および有効性を評価する第1/2相臨床試験。この試験では抗PD-1抗体または抗CTLA-4抗体による治療歴のある患者を除外している。同試験の第1相用量漸増パート(epacadostat 25、50、100mgを1日2回+キイトルーダ2mg/kgを3週間ごとに1回静脈内投与およびepacadostat 300mgを1日2回+キイトルーダ200mgを3週間ごとに1回静脈内投与)および第1相用量拡大パート(epacadostat 50、100および300mgを1日2回+キイトルーダ200mgを3週間ごとに1回静脈内投与)への登録は終了してる。
SCCHN・UC・RCCで有望な有効性
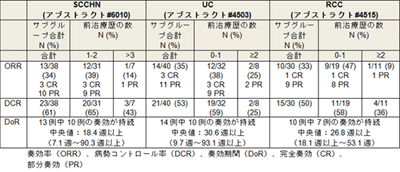
今回、転移性または再発性扁平上皮頭頸部がん(SCCHN)・進行性尿路上皮膀胱がん(UC)・進行性腎細胞がん(RCC)のコホートで得られた最新の有効性データと、全試験対象集団(すべてのコホート)のプールされた安全性解析データ(第2相臨床試験)を発表。SCCHNでは、奏効率(ORR)34%、奏功期間(DoR)は中央値:18.4週以上(7.1週~90.3週以上)で13例中10例が奏功を持続している。UCでは、ORR38%、DoRは中央値:30.6週以上(9.7週~93.1週以上)で14例中10例が奏功を持続し、RCCではORR33%、DoRは中央値:26.8週以上(18.1週~53.1週以上)で10例中7例が奏功を持続している。
安全性については、第2相臨床試験ECHO-202の安全性解析対象集団である進行がん患者294例について、新たな情報に基づきプール解析を実施。治療との関連性が否定できない有害事象は患者の67%(n=197/294)に認められた。最も高頻度に認められた有害事象は、倦怠感(29%)、発疹(17%)、悪心(11%)および掻痒感(10%)。グレード3以上の有害事象は患者の18%(n=52/294)に認められ、最も高頻度のものはリパーゼ上昇(無症候性)(4%)および発疹(3%)だった。また、有害事象により患者の4%が治療を中止した。epacadostatとキイトルーダ併用療法の安全性データは、これまでに報告された第1相臨床試験ECHO-202の安全性プロファイル、およびキイトルーダ単独療法の安全性プロファイルと一致している。
これらの結果について、Incyte社のDr. Steven Stein氏は「第1/2相臨床試験であるECHO-202の複数種のがんにおけるコホートで、この併用療法は有望な有効性と安全性を示しました。このようなデータを報告することができうれしく思います」とコメントしている。
▼関連リンク
・MSD株式会社 ニュースリリース






