ALSの治療標的となる分子経路を同定
京都大学iPS細胞研究所(CiRA)は5月25日、ALS患者由来iPS細胞を用いて治療薬探索のための薬剤スクリーニングを行い、ALSの治療標的となる分子経路とALS運動ニューロンの細胞死を抑える既存薬を同定したと発表した。この研究は、CiRA増殖分化機構研究部門の今村恵子特定拠点助教と井上治久教授らによるもの。研究成果は、米科学誌「Science Translational Medicine」誌にオンライン公開されている。
画像はリリースより
ALSは、運動ニューロンが進行性に変性することで、筋萎縮と筋力低下が生じる原因不明の疾患。そのメカニズムは詳しく知られておらず、まだ十分な治療法はない。全国で約9,200人の患者がおり、そのほとんどは孤発性だが、約5%が家族性であり、そのうちの約20%にSOD1遺伝子変異を伴う。その他、TDP-43遺伝子変異やC9orf72遺伝子内のくり返し配列の伸長などの遺伝要因が知られている。
Src/c-Ablのリン酸化を抑制する「ボスチニブ」
研究グループは、ALSの治療薬を探索するため、患者由来のiPS細胞から運動ニューロンを作製してALSの病態を再現し、その病態を改善する化合物のスクリーニングを実施。まず、SOD1遺伝子に変異をもつ家族性ALS患者から作製したiPS細胞、遺伝子変異を修復したiPS細胞と健康な人から作製したiPS細胞(対照群)に、Lhx3、Ngn2、Isl1という3つの転写因子を加えて運動ニューロンへと分化させた。その結果、患者由来運動ニューロンでは異常に折りたたまれたタンパク質が蓄積し、細胞死を起こしやすいことがわかったという。
そこで、ALS患者の運動ニューロンの細胞死を抑制する化合物を見つけるため、SOD1変異を有する家族性ALS患者由来運動ニューロンを用いて、細胞死を標的としたスクリーニング系を構築。既存薬を含む1,416個の化合物について、運動ニューロンの細胞死を抑えるかどうかのスクリーニングを行ったところ、27個の薬が細胞死を強く抑えた。また、そのうち14個がSrc/c-Ablというタンパク質の分子経路に関連していることが判明。そこで、細胞内のSrc/c-Ablを調べてみると、家族性ALS患者iPS細胞由来運動ニューロンでは、リン酸化されたSrc/c-Ablが増えており、細胞死に関連していることが明らかになったという。
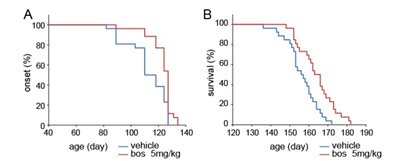
研究グループはさらに、運動ニューロンの細胞死を強く抑え、慢性骨髄性白血病の治療薬として用いられている「ボスチニブ」という既存薬に注目。これは、Src/c-Ablのリン酸化を抑制する既存薬であり、この物質がどのようにしてALS運動ニューロンの細胞死を抑制するのかについてのメカニズムを調べた。その結果、不要なタンパク質を分解する働きであるオートファジーを促進し、ALSの病態のひとつである異常に折りたたまれたタンパク質を減らすことがわかった。そして同剤を、SOD1変異を有するALSマウスに投与したところ、ALSの発症を遅らせ、生存期間も延長。ALSマウス脊髄中の折りたたみ異常を呈するタンパク質の量を減少したという。
最後に、TDP-43遺伝子変異あるいはC9orf72リピート伸長を有する家族性ALS患者由来iPS細胞から作製した運動ニューロンや、孤発性ALS患者由来iPS細胞から作製した運動ニューロンの一部でも、ボスチニブが細胞死を抑制することが判明したとしている。今後、ALSの治療へと応用するためには、生体内での薬の有効濃度や髄液への移行性・安全性などを詳細に調べる必要がある、と研究グループは述べている。
▼関連リンク
・京都大学iPS細胞研究所 ニュース






