アレルギーの発症に関与する好塩基球内の蛋白分解酵素
東京医科歯科大学は10月26日、好塩基球に選択的に発現する蛋白分解酵素であるmMCP-11の欠損マウスを作製・解析した結果、mMCP-11が慢性アレルギー炎症の誘導に重要な役割を果たすことを明らかにしたと発表した。この研究は、同大学大学院医歯学総合研究科免疫アレルギー学分野の山西吉典講師、烏山一教授(副学長・理事)のグループによるもの。研究成果は「Blood」オンライン版に10月27日付で掲載されている。
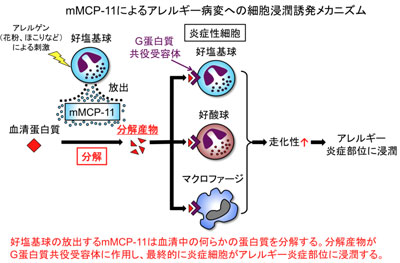
画像はリリースより
アトピー性皮膚炎、喘息、花粉症などのアレルギーは日本国内において約3~4割もの人が罹患し、その数は年々増加傾向を示しているが、根本的な治療法・予防法は未だ確立されていない。白血球の0.5%を占める希少な免疫細胞である好塩基球が、アレルギー反応において、他の免疫細胞(アレルギー反応の主役ともいえる肥満細胞やT細胞など)とは異なるユニークかつ重要な役割を果たしていることが最近の研究で分かってきていた。研究グループは、これまでにマウスの慢性アレルギー皮膚炎症モデルを用いて、好塩基球がIgE依存的慢性アレルギー炎症を引き起こす主役であることを突き止めている。
今回は、好塩基球のみが選択的に産生・放出する蛋白分解酵素のひとつであるmMCP-11に着目。mMCP-11は通常、好塩基球の内部に貯蔵されているが、アレルゲンなどで好塩基球が刺激を受けると、外部に放出されることがわかっている。
ヒト好塩基球に存在する類似の蛋白分解酵素β-tryptaseにも同様の細胞走化作用
研究グループはmMCP-11欠損マウスを作製して解析。IgE依存的慢性アレルギー炎症を誘発すると、mMCP-11の存在する野生型マウスに比べて、皮膚の腫脹・血管透過性亢進・炎症性細胞(好塩基球、好酸球、好中球、マクロファージ)浸潤といった炎症兆候が半減していた。人工的に作製したmMCP-11をマウスの耳に皮内注射すると、皮膚の腫脹と炎症性細胞浸潤が起こったという。
加えて、試験管内で好塩基球、好酸球、マクロファージを mMCP-11で刺激すると細胞の走化性が高まり、mMCP-11の存在するほうへと細胞が引き寄せられる現象が観察された。この細胞の走化現象は、血清中に存在する何らかの蛋白質が蛋白分解酵素であるmMCP-11によって切断され、その切断後の分解産物が誘発因子となって引き起こされることが判明。分解産物は最終的に好塩基球、好酸球、マクロファージの細胞表面に存在するG蛋白質共役受容体に作用して、これら細胞の走化性を高めることも明らかとなった。
これらの結果から、好塩基球が蛋白分解酵素mMCP-11を使って、これまで知られていなかった全く新しいメカニズムで炎症性細胞を炎症部位に呼び寄せて、慢性アレルギー炎症を引き起こすことが明らかとなった。また同研究では、ヒト好塩基球に存在する類似の蛋白分解酵素β-tryptaseにも同様の細胞走化作用があることも確認。今回の研究成果を起点として、好塩基球の産生・放出する蛋白分解酵素を標的としたアレルギー疾患の新規治療法・予防法開発への道筋が拓けることが多いに期待されると、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース




