2015年7月に難病指定、治療法確立されず
千葉大学は8月16日、同大学病院が世界で初めての遺伝子治療研究となる、家族性レシチンコレステロールアシルトランスフェラーゼ(LCAT)欠損症を対象とした第一種再生医療臨床研究の実施に関して、8月8日に厚生労働省より承認を得たと発表した。
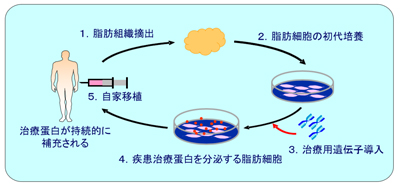
画像はリリースより
家族性LCAT欠損症は、LCATを作り出す遺伝子の異常でLACT蛋白を体の中に作り出すことができない疾患。LCATが十分に働くことができないため、血液中の善玉コレステロールが著しく減少し、余分なコレステロールが腎臓や目などに蓄積し、腎機能障害、角膜混濁、溶血性貧血などの障害を起こす。比較的まれな遺伝疾患であり、治療法が確立されていない難病で、2015年7月1日付で厚労省より難病指定されている。
千葉大学病院では、脂肪細胞がヒトの細胞の中でも特に寿命が長く、またがん化などの変化も生じにくいなどの特徴に着目し、難病を治療するために蛋白を分泌するよう加工した治療用遺伝子導入ヒト脂肪細胞の実用化研究を進めてきた。今回の臨床での治療研究は、2014年より施行された再生医療等安全性確保法の下、千葉大学病院と千葉大学発バイオベンチャーのセルジェンテック株式会社が日本医療研究開発機構(AMED)から支援を受け、患者を対象とした臨床試験を進める。
難病治療用の加工ヒト脂肪細胞研究で、遺伝子細胞医薬品の承認・実用化へ
この治療法は、家族性LCAT欠損症の患者の脂肪組織から採取した脂肪細胞を体外で培養し、遺伝的に欠損しているLCAT遺伝子を導入、LCAT蛋白を造り出すように加工したのちに患者自身へ再び移植し、正常なLCAT蛋白を持続的に体内へ補充する。この技術は、今後、家族性LCAT欠損症のみならず血友病やライソゾーム病など多くの難病治療法開発につながると期待されている。
同病院は、実用化へ向けた研究を行い、将来的にはインスリンを補充し糖尿病の治療に役立てることを目指した研究を進める予定。セルジェンテック社は、これらの研究成果に基づき、難病治療用の加工ヒト脂肪細胞の研究開発を進め、遺伝子細胞医薬品としての承認・実用化を目指すとしている。
▼関連リンク
・千葉大学 プレスリリース




