角膜上皮細胞の分化を規定する転写因子の同定を試みる
京都府立医科大学は4月28日、ヒト角膜上皮分化を規定している新分子を発見したと発表した。この研究は、同大学特任講座 感覚器未来医療学の北澤耕司助教、木下茂教授、京都大学iPS細胞研究所(CiRA)の升井伸治講師らのグループによるもの。同研究成果は、米科学雑誌「Cell Reports」のオンライン版に4月28日付けで公開されている。
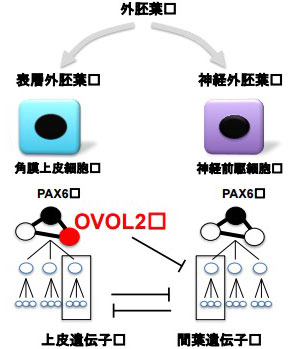
画像はリリースより
胚が発生する過程で、外胚葉は神経外胚葉と表層外胚葉に分かれ、後者から角膜は作られる。神経外胚葉由来の神経細胞と表層外胚葉由来の角膜上皮細胞はどちらも同じマスター転写因子PAX6が働いていることが知られており、遺伝子発現上は似た細胞といわれている。これらの細胞を分けるメカニズムを明らかにできれば、iPS細胞などから角膜上皮細胞を作出する技術開発に貢献できると考えられるという。
近年、細胞の分化には転写因子が大きな役割を果たすことがわかってきており、神経外胚葉由来の細胞では分化を規定する転写因子が報告されている。しかし、表層外胚葉由来細胞に関する報告は少なく、今回の研究では角膜上皮細胞の分化を規定する転写因子の同定を試みたという。
難治性の角膜疾患に対して、iPS細胞からの分化誘導の高効率化に期待
研究グループは、CiRAの升井講師が独自に開発したiPS干渉法を用いて、OVOL2を含む6つの転写因子セットが、ヒト角膜上皮の性質を決定しているキーとなる因子であることを見出した。このセットをヒト皮膚線維芽細胞に導入することによって、2週間で角膜上皮特異的タンパク質を発現している細胞を誘導することに成功したという。
また、角膜上皮細胞においてOVOL2をノックダウンさせると、角膜上皮の重要な機能の1つである異物の侵入をブロックするバリア機能が大きく低下。さらに、その維持メカニズムとして、上皮間葉転換を介していることがわかったという。
現在、Stevens-Johnson症候群、眼類天庖蒼、熱化学外傷などの角膜上皮幹細胞が枯渇してしまうような最重症眼表面疾患に対しては、培養口腔粘膜上皮細胞を用いた再生医療が行われている。しかし、培養口腔粘膜上皮は角膜上皮とは性質が異なるため、移植手術の効果が限定的だ。また、iPS/ES細胞から角膜上皮細胞への分化誘導は培養期間が長く、誘導効率が低いといった課題がある。今回の研究結果により、角膜上皮細胞の特異性を維持している分子を解明し、短期間で高効率に高品質な角膜上皮細胞を作製できることが期待されると、研究グループは述べている。
▼関連リンク
・京都府立医科大学 プレスリリース






