世界初、分子メカニズム解明
岡山大学は2月17日、おもに肝臓に発現する酵素である「PEMT」(ホスファチジルエタノラミン-N-メチルトランスフェラーゼ)の発現の低下が、脂肪肝・非アルコール性脂肪肝炎(NASH)を進めることを明らかにし、その分子メカニズムを世界で初めて解明したと発表した。この研究は、同大学大学院医歯薬学総合研究科(医)腎・免疫・内分泌代謝内科学分野の和田淳教授、中司敦子助教らの研究グループによるもの。研究成果は、英国の科学雑誌「Scientific Reports」電子版に英国時間の同日付けで掲載された。
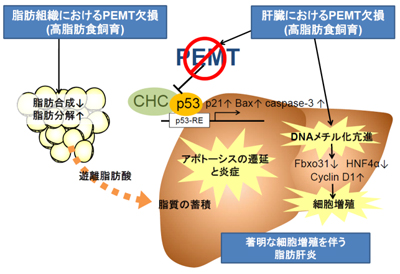
画像はリリースより
近年、メタボリックシンドロームや糖尿病が増加し、これに伴う脂肪肝や脂肪肝炎が注目されてきた。一方で、肥満や糖尿病がなくても起こる脂肪肝・脂肪肝炎はあまり知られていない。
これまでPEMT遺伝子の一塩基多形を持つ人は、NASHのリスクがあると報告されていた。PEMTの働きの低下によって、肝臓から中性脂肪が肝外への放出が低下するためと考えられてきたが、炎症・線維化がなぜ起こるのか、そして脂肪肝炎に進展するメカニズムは解明されていなかった。
脂肪肝、脂肪肝炎の革新的な治療法開発に期待
研究グループは、PEMTを欠損したマウスを高脂肪高蔗糖食で飼育。野生型マウスと比べてPEMT欠損マウスは肥満が抑制されるが、早期から著しいNASHを発症し、多発性肝腫瘤が出現することを発見した。患者においても、単純性脂肪肝よりもNASHの肝臓でPEMTの発現は低下しており、肥満のない痩せたNASHにおいてPEMT発現がより低下していることを見出したとしている。
また、研究によりPEMTは、クラスリン重鎖(CHC)とp53という物質が複合体を形成することがわかった。さらに、PEMTが欠損するとCHCとp53がアポトーシスに関連した遺伝子の転写を活発化させ、肝細胞アポトーシスが強まり、炎症が起こるというメカニズムを解明。PEMT欠損によりFbxo31、HNF4αという遺伝子のDNAメチル化が亢進し、両遺伝子の発現が抑制されることによって、細胞増殖に関係するcyclinD1の発現が著しく増強することも新たに発見した。
今回の研究において、PEMTの発現低下により、脂肪肝に加えて、炎症や線維化が強まって脂肪肝炎へと進行する分子メカニズムが初めて解明された。今後、肝組織や血球細胞を用いてPEMTの量や働きを測定したり、一塩基多形の有無を調べたりすることで、脂肪肝から脂肪肝炎へと進行するリスクの高い症例を判断することができる。さらに、これまでにない革新的な治療法の開発へと研究を進めることが可能になる、と研究グループは述べている。
▼関連リンク
・岡山大学 プレスリリース






