血管が作るDel-1分子による炎症コントロールとメカニズム
新潟大学は10月19日、同大歯学部の前川知樹助教が、米国・ペンシルベニア大学のHajishengallis George教授、ドイツ・ドレスデン工科大学のChavakis Triantafyllos教授との日欧米国際共同研究を行い、Del-1が炎症反応を抑制するメカニズムと歯周病モデルにおけるDel-1の骨破壊への影響を明らかにしたと発表した。
画像はリリースより
さまざまな病原体は多岐にわたる感染症を引き起こすが、病態増悪の共通因子として炎症反応がある。慢性炎症の代表疾患である歯周炎は、歯肉炎症と続発する歯槽骨の破壊を特徴とし、人類史上最も多い感染症であるとされている。歯周病は歯を失う一番の事由かつ全身疾患へ波及する炎症疾患だが、有効な治療法は確立されていない。
新潟大学歯学部は、口腔に関するこれら諸課題を解決する「ミッションの再定義」を掲げ、高度口腔機能教育研究センター(センター長・学部長 前田健康教授)を設立。新大歯学部では同センターを枢軸に据え、優れた若手が独自のアイデアで研究できる組織改革を行っている。今回の研究は、その初めての成果になるという。
慢性炎症性疾患の治療基盤となる可能性を示唆
Del-1は、血管内皮細胞が主に産生し、粘膜や中枢神経系の炎症と好中球の遊走を制御している。今回の研究では、Del-1が破骨細胞とその前駆細胞表層のMac-1受容体に作働し、破骨細胞の骨吸収活性を減弱することと、前駆細胞からの分化を抑制することを明らかにした。続いて、Del-1を歯周炎のサル歯肉に投与したところ、患部組織の炎症を抑えたことに加え、破骨細胞の数を減らすことにも成功。さらに、歯周病の進行指標である歯肉ポケット深さや骨吸収指数もそれぞれ改善させることができた。これらの結果は、ヒトの血管に備わる分子を用いて、歯周炎を治療できる可能性を示しているという。
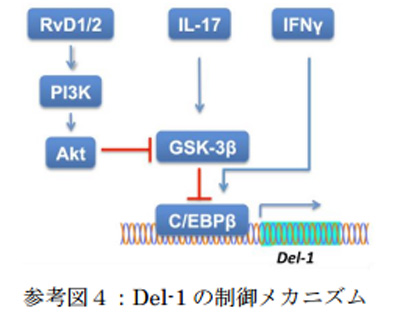
そこで、治療標的の炎症部位へDel-1を効率よく誘導させる方法を調べた。研究グループは、炎症組織ではDel-1がほとんど産生されていないことに着目。炎症が進むと、サイトカインIL-17が多量に産生され、転写因子C/EBPβを介してDel-1産生が制御されることを見出した。さらに、抗炎症性代謝産物として知られていたレゾルビンは、このIL-17を抑制することでDel-1の産生経路を解放し炎症抑制効果を発揮すること、すなわちレゾルビンの炎症部位への投与がDel-1を介した患部炎症の寛解に効果的であることを示したという。
今後は、歯周炎を含む炎症性疾患に対して、Del-1やレゾルビン等のヒト由来分子をコントロールすることで、治療に繋げる将来展望を検索していく予定だ。
▼関連リンク
・新潟大学 プレスリリース




