KRAS阻害薬への初期耐性機序、半数以上の患者で未解明
がん研究会は1月10日、樹立した大腸がん患者由来細胞株を用いて、KRAS変異大腸がんの分子標的薬に対する耐性メカニズムを発見したと発表した。この研究は、同会がん化学療法センター基礎研究部の片山量平部長、丸山航平氏らの研究グループによるもの。研究成果は、「npj Precision Oncology」に掲載されている。
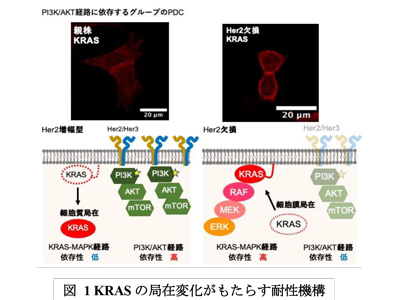
画像はリリースより
(詳細は▼関連リンクからご確認ください)
KRAS変異陽性の大腸がんの薬物療法では、BRAF変異大腸がんで使用されるBRAF阻害薬のようにがん遺伝子を標的とした分子標的薬が承認されておらず、1960年代から使用されている古典的な殺細胞性の抗がん剤に抗血管新生阻害薬を併用する薬物治療が行われている。この背景にはKRASを特異的に阻害する分子標的薬の開発が遅れてきたことが挙げられる。
しかし、近年KRAS特異的な阻害薬が開発され臨床応用に向けた研究開発が進められており、大きな関心が寄せられている。最初に開発されたKRAS G12C変異特異的阻害薬ソトラシブの臨床試験では、肺がんと比較し大腸がんでの奏効率は顕著に低く、単剤での有効性は限定的だった。この最初から耐性を示す原因に関しては複数の研究グループが報告を行っており、大腸がんでは受容体型チロシンキナーゼのEGFRがKRAS阻害薬を処理すると活性化し、KRAS阻害薬耐性の原因となっていることが報告されている。実際に、EGFR阻害薬セツキシマブとKRAS阻害薬アダグラシブとの併用臨床試験では奏効率が47%と大幅に改善され、米国では臨床での使用が承認されている。
一方で半数以上の患者での初期耐性機序はほとんど明らかではなく、大腸がんに対する初期耐性機序の理解は十分とは言えない。そこで研究グループは、独自に患者検体から樹立したKRAS変異大腸がん細胞株を用いてKRAS阻害薬に対する初期耐性機序の解析を行うこととした。
残余組織片から患者由来細胞株を樹立、KRAS阻害薬への初期耐性機序を解析
初めに、がん研究会の倫理審査委員会承認済みのプロトコールに従い同意の得られた大腸がん患者の手術残余組織片から患者由来細胞株(PDC)の樹立を行った。その後、手術検体のシークエンス解析からKRAS変異を特定し、KRAS変異陽性の大腸がんPDCを中心に用いてKRAS阻害薬への初期耐性機序の解析を行った。
「EGFR活性化」もしくは「PI3K/AKT経路」に依存する耐性機序のグループが判明
樹立したPDCはKRAS阻害薬単剤には初期耐性を示し、KRASのみに依存した細胞増殖や生存は示さず、KRAS阻害薬の存在下では別のシグナル経路や因子が代償的に活性化することで耐性に寄与する可能性が示唆された。そこで薬剤ライブラリーを用いたスクリーニングと遺伝子変異解析等を実施し、耐性機序を探索した。その結果、「KRAS阻害薬の存在下で受容体型チロシンキナーゼであるEGFRの活性化に依存するグループ」と「細胞の生存や増殖、代謝に関連するPI3K/AKT経路に依存するグループ」の少なくとも2つに分けられることが判明した。
KRAS変異+Her2増幅の患者細胞、KRAS局在変化しPI3K/AKT経路活性化
新たな耐性機序の解明のため、後者のグループに属するPDCに注目し、詳細な解析を実施した。その内の1つのPDCではKRAS変異の他にHer2遺伝子の増幅とPI3Kの変異を有しており、PI3K/AKT経路が強力に活性化していることがわかった。このPDCではPI3KとmTORを同時に阻害することで強い増殖抑制効果が得られ、Her2増幅によってKRAS変異を有しながらもPI3K/AKT経路に依存していることが示唆された。
さらに興味深い点として、Her2を遺伝子ノックアウトにより欠損させた細胞では、KRAS~MAPK経路への依存性が高くなることがわかった。そこで、このPDCが依存するシグナル経路のスイッチがどのようなメカニズムで起こったのかを解析した。その結果、本来細胞膜で活性化するKRASがこのHer2の増幅があるPDCでは細胞質に多く局在し、Her2をノックアウトした細胞では細胞膜に局在することが判明した。
KRAS阻害薬治療の効果に基づく患者の層別化に貢献できる可能性
今回の研究によってHer2増幅型のKRAS変異大腸がんではKRASの局在異常によってKRAS~MAPK経路の依存性が低下し、KRAS阻害薬への耐性に寄与する可能性が示された。また、遺伝子変異やタンパク質発現変化だけでは分からないタンパク質の細胞内局在の変化によって誘導される耐性機序を見出すことに成功した。
「今回の発見により、今後KRAS阻害薬を用いた治療法が大腸がんで承認された場合でも、治療初期から十分な治療効果が期待できる患者とそうではない可能性が高い患者の層別化に貢献できる可能性が期待される」と、研究グループは述べている。
▼関連リンク
・がん研究会 ニュースリリース



