デュシェンヌ型筋ジストロフィー、エクソン53以外を標的とした薬剤開発が必要
国立精神・神経医療研究センター(NCNP)は1月10日、アンチセンス核酸医薬品であるデュシェンヌ型筋ジストロフィー(DMD)治療薬(ブロギジルセン:NS-089/NCNP-02)を用いた医師主導治験(First In Human試験)において、画期的なジストロフィン回復を実現したと発表した。この研究は、NCNP神経研究所遺伝子疾患治療研究部の青木吉嗣部長、邦武克彦研究員、トランスレーショナル・メディカルセンターの小牧宏文TMCセンター長、日本新薬株式会社らの研究グループによるもの。研究成果は、「Cell Reports Medicine」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
DMDは、ジストロフィン遺伝子の変異が原因で、筋の細胞膜からジストロフィンタンパク質が失われ、徐々に筋力低下が進む難病で、男児に発症する。
「エクソン・スキップ治療」は、アンチセンス核酸と呼ばれる短いDNAのような合成核酸を用いて、メッセンジャーRNA前駆体から成熟メッセンジャーRNAが作られる過程で、タンパク質に翻訳されるエクソン領域の一部を人為的に取り除く(スキップする)ことで、アミノ酸読み取り枠のずれを修正する治療法である(イン・フレーム化という)。この結果、正常なジストロフィンに比べると、タンパク質の一部が短縮するものの、機能を保ったジストロフィンが発現して筋機能の改善が期待できる。
この治療でスキップの対象となるエクソンは患者の変異形式に応じて異なり、現在までに、日本では、NCNPと日本新薬が共同で見出したビルトラルセンを有効成分としたエクソン53スキップ薬であるビルテプソ(R)点滴静注250mgが製造販売承認を取得しているが、エクソン53スキップ薬が適応にならない患者に対して、別のエクソンを標的とした薬剤の開発が喫緊の課題となっている。
エクソン44スキップ薬「ブロギジルセン」、非臨床試験で高い有効性
ブロギジルセンは、NCNPと日本新薬が共同で開発した世界初のエクソン44スキップ薬である。モルフォリノ核酸が本来有する高い安全性に加えて、特許出願技術である新規高活性配列探索法を用いて開発したデュアルターゲティング(配列連結型)モルフォリノ核酸製剤であり、高いエクソン・スキップ活性を有している。これまでに得られた非臨床試験の結果からは、エクソン44スキップに応答する変異形式のDMD患者細胞における高い有効性が確認されていた。
医師主導治験実施、6人の患者で平均20.55%のジストロフィンタンパク質発現
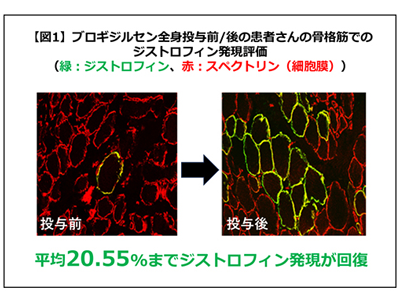
今回の医師主導治験(UMIN:000038505、ClinicalTrials.gov:NCT04129294)は、NCNP病院と鹿児島大学病院で6人のDMD患者に対して行われ、主要評価項目である安全性のほか、ブロギジルセン投与後の薬物動態、ジストロフィンタンパク質の発現確認、運動機能評価などの有効性について検討を行った。結果として、ブロギジルセンの全身投与により、平均20.55%のジストロフィンタンパク質の発現が認められた。
運動機能は維持または改善傾向、有害事象による投与中止はなし
また、ノース・スター歩行能力評価スコアを含め、運動機能の維持または改善傾向が示唆された。これらの結果から本剤は、DMDに対する治療効果が期待される。今回の治験を通じて、有害事象の発生による投与中止例はなかった。
身体に負担をかけないエクソン・スキップ治療効果検証方法、尿中細胞を用いて開発
研究グループはこれまでに、尿の中に含まれる幹細胞(以下、尿中細胞)をダイレクト・リプログラミング法で骨格筋細胞へ変換し、身体に負担をかけることなく、かつ効率的にエクソン・スキップ治療の効果を実験皿の上で検証する方法を既に確立していた。そこで、今回の治験でも、すべての患者より尿中細胞を採取し、この方法を用いて、ブロギジルセンの効果を検証したところ、実際の全身投与で有効だった患者では、その尿中細胞由来の骨格筋細胞においても、同様に有効でジストロフィンの発現上昇が見られた。これまでの治験では、苦痛を伴う筋生検によって得られる骨格筋がエクソン・スキップ治療の有効性評価のためには必須だった。しかし、将来のDMD関連の治験においても継続的に尿中細胞を用いた評価が有用であることが示せれば、苦痛のない尿中細胞を主要評価項目とする治験実施も期待される。
日常診療の治療反応性マーカーとなり得るタンパク質も判明
また、DMDに対するエクソン・スキップ治療では、日常診療で使いやすい治療効果判定の血中マーカーは確立されていないのが現状である。そこで、今回の治験ではブロギジルセンの投与前後の血漿を用いて、タンパク質の網羅的な発現解析を行った。その結果、以前よりDMDで高値であることが知られていたタイチン(TTN)、ミオメシン2(MYOM2)、ミオシン軽鎖PF(MYLPF)が、いずれもジストロフィンの回復に伴い、低下することがわかった。さらに、これまでDMDではほとんど注目されてこなかったタンパク質である繊毛神経栄養因子(CNTF)の上昇、プロテインアルギニンデイミナーゼ2型(PADI2)の低下も見られた。これらのタンパク質は、日常診療の治療反応性マーカーとなり得るばかりか、今後のDMD関連治療薬の治験における測定項目となることが期待される。
今回の医師主導治験の結果も踏まえ、日本新薬が臨床試験を引き継ぎ、上市に向けて今回の医師主導治験継続投与試験とグローバル第2相試験を実施している。
▼関連リンク
・国立精神・神経医療研究センター プレスリリース






