劇的に効く治療薬がない心不全、ミトコンドリア機能を維持する機構に着目
大阪大学は12月18日、Bcl2-L-13によるマイトファジーの誘導が負荷のかかっている心臓の機能維持に重要な役割を果たしていること、マイトファジーの誘導にはAMPKa2によるBcl2-L-13のリン酸化が重要であることを明らかにしたと発表した。この研究は、同大大学院医学系研究科の村川智一助教、坂田泰史教授(循環器内科学)、英国キングスカレッジロンドン、愛媛大学ほかの研究グループによるもの。研究成果は、「Cell Reports」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
心不全は日本を含む先進国において主要な死亡要因の1つである。心不全を発症した患者の5年生存率は約50%と、全がん患者の平均よりも低い状態が続いている。その理由として、劇的に治療効果を発揮する薬剤が不足していることが挙げられ、新たな治療戦略の開発が望まれている。
ミトコンドリアは、細胞内でのエネルギー産生を担う細胞内小器官である。心臓は、エネルギーを大量に消費するため、ミトコンドリアを大量に含んでいる。そのため、心機能の維持には、ミトコンドリアの機能を正常に保つことが重要である。
障害ミトコンドリア除去機構マイトファジー、哺乳類での必須分子はBcl2-L-13
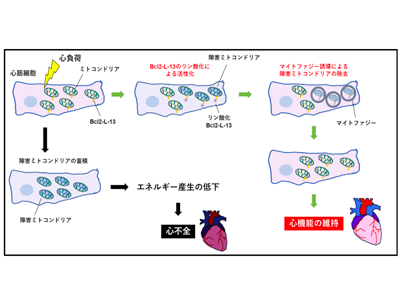
研究グループは、心不全状態の心臓において機能の低下した障害ミトコンドリアが蓄積していることに着目し、これらを効率よく分解・除去することができれば心臓の機能を維持できるのではないかと考えた。障害ミトコンドリアの分解・除去機構にはマイトファジーと呼ばれる仕組みが働いている。研究グループはこれまでに、酵母においてマイトファジーに必須の分子であることが知られているAtg32と同様の機能を持つ分子として、Bcl2-L-13を同定した。Bcl2-L-13は哺乳類細胞においてマイトファジーを誘導することを見出していたが、その生体内、特に心臓における役割は不明だった。
Bcl2-L-13欠損マウス、TAC手術による軽い負荷で心機能低下・マイトファジー増加は抑制
研究グループは、「心不全が起こるメカニズムにおいてBcl2-L-13がどのような役割を果たしているのか」について検討するため、Bcl2-L-13を欠損した遺伝子改変マウスおよび、Bcl2-L-13を活性化できない遺伝子改変マウスを作製し、大動脈を狭窄させる手術(TAC手術)を施すことで心臓を高血圧状態に置いた。
その結果、対照群(Bcl2-L-13が機能するマウス)では左心室の収縮能が低下しない程度の軽い負荷でも、遺伝子改変マウスでは心機能の低下が見られた。また、対照群で見られた負荷によるマイトファジーの増加は遺伝子改変マウスでは抑制されており、ミトコンドリアの機能も低下していた。
AMPKa2によりリン酸化されたBcl2-L-13、マイトファジー誘導し心機能を維持と判明
さらに、種々のリン酸化キナーゼをノックダウンしてスクリーニングを行うことで、AMPKa2というリン酸化キナーゼがBcl2-L-13をリン酸化し、活性化させることを見出した。
これらの結果より、Bcl2-L-13によるマイトファジーの誘導が圧負荷状態にある心臓の機能維持に重要な役割を果たしていること、マイトファジーの誘導にはAMPKa2によるBcl2-L-13のリン酸化が重要であることが明らかとなった。
AMPKa2活性高めマイトファジー亢進させる心不全治療薬の開発に期待
今回の研究成果により、AMPKa2の活性を高め、ミトコンドリア分解を担うマイトファジーを亢進させることで、ミトコンドリアの機能を維持し、心不全の発症を抑制できる可能性が示唆された。「マイトファジーを制御する心不全治療薬は現時点で存在しないが、この成果をもとに新しい心不全治療薬が開発されれば、心不全患者を減らしたり、生存率を改善させたりすることが期待される」と、研究グループは述べている。
▼関連リンク
・大阪大学 ResOU




