原因タンパク質「IRF5」を突き止めることに成功
九州大学は5月12日、同大大学院薬学研究院薬理学分野の井上和秀主幹教授と津田誠准教授を中心とする研究グループが、神経障害性疼痛の原因タンパク質を同定することに成功したと発表した。
この研究成果は、最先端・次世代研究開発支援プログラムおよび独立行政法人 科学技術振興機構(JST)戦略的創造研究推進事業チーム型研究(CREST)によるもの。英科学誌「Nature Communications」オンライン版に現地時間5月13日付で掲載されている。
画像はプレスリリースより
研究グループは、これまでに脳や脊髄に存在する免疫細胞と呼ばれるミクログリアが、神経損傷後の脊髄では過度な活性化状態になり、炎症性物質を産生、慢性的な痛みを引き起こしていることを明らかにしていた。
ミクログリアは細胞の働きを調節するタンパク質の増加で活性化するが、特に細胞の外にあるATPで刺激されるP2X4受容体が、神経障害性疼痛の発症において非常に重要な役割を果たしていると考えられることも発表している。
P2X4受容体は、神経の障害後にミクログリアだけで増え、この受容体を薬物で遮断すると痛みが緩和されることも分かっているが、どのようなメカニズムでこのP2X4受容体がミクログリアの中だけに増加するのかは、不明なままだった。
IRF5がP2X4受容体の調節に必要な遺伝子領域に作用
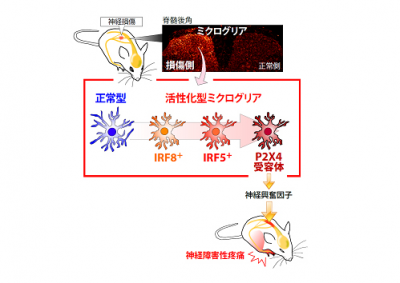
今回、研究グループは、神経を損傷させたマウスの脊髄で、インターフェロン調節因子ファミリーに属し、細胞の核内にあるDNAに結合してさまざまな分子の発現を調節、免疫制御に関わっているタンパク質の「IRF5」が、ミクログリアの中においてのみ増えることを発見した。またこの増加は、「IRF8」によって調節されていることも分かったという。
IRF5を作り出せないようにしたノックアウトマウス(IRF5遺伝子欠損マウス)では、神経損傷後の痛みが弱くなることも確認。さらに、IRF5がP2X4受容体の調節に必要な遺伝子領域に作用し、P2X4受容体を増やすように働いていることを突き止めたという。
このことから、神経損傷後には、IRF8によってミクログリアで増えるIRF5がP2X4受容体の増加を招き、神経障害性疼痛の発症につながるという一連の流れが示された。この成果は、慢性疼痛メカニズムの全容解明に向けた大きな前進であり、疼痛治療薬開発への応用が期待される。(紫音 裕)
▼外部リンク
九州大学 プレスリリース
http://www.kyushu-u.ac.jp/pressrelease/2014/
Transcription factor IRF5 drives P2X4R+ reactive microglia gating neuropathic pain
http://www.nature.com/ncomms/2014/140513/




