心筋への血流再開後に大量の活性酸素発生で起こる障害、有効な治療法は?
慶應義塾大学は10月30日、心筋梗塞が引き起こす有害な活性酸素の除去機能が徐々に低下するメカニズムを特定したことを発表した。この研究は、同大医学部内科学教室(循環器)の市原元気助教(研究当時)、佐野元昭准教授、同スポーツ医学総合センターの勝俣良紀専任講師と、京都大学大学院医学研究科の杉浦悠毅特定准教授の共同研究グループによるもの。研究成果は、「Circulation Research」に掲載されている。
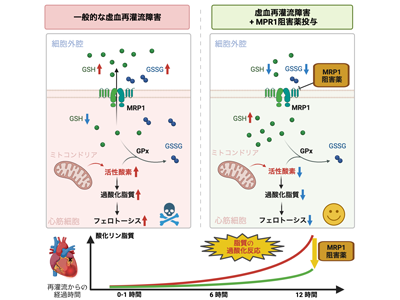
画像はリリースより
(詳細は▼関連リンクからご確認ください)
心筋梗塞(虚血性心疾患)は、全世界において死因の上位を占める重篤な疾患。近年、血行再建手術やカテーテル治療の発達によって、心筋梗塞患者の救命率は大幅に改善した。一方で、救命はできたものの、心臓のポンプ機能が十分に回復せずに身体機能が低下し、日常生活に著しい制限を余儀なくされる患者も多くいる。心筋梗塞後の心不全に苦しむ患者が発生する要因として重要なのが、虚血再灌流障害だ。虚血再灌流障害とは、虚血に陥った心筋の血流を再開させた際に、急激な再酸素化に伴って多量の活性酸素が生じ、これが細胞内の種々のタンパク質を変性させてしてしまう現象である。心臓の虚血再灌流障害は、カテーテルや手術による虚血心筋の完全な救済にあたって大きな障壁となっているものの、いまだに確立した治療法はない。
心筋間質の代謝物質を連続的に回収し、MRP1を介したグルタチオン放出の関与を発見
研究グループは今回、動物(ラット)の心臓を用いて虚血再灌流を再現し、その過程で生じる代謝物質の変動を生きたままの状態で連続的かつ包括的に解析した。従来の研究手法では、虚血再灌流後の心筋組織を採取し、種々の代謝物質やタンパク質を測定することで治療の標的となる分子を探索した。この方法では、時間とともにダイナミックに変化する心筋の代謝状態を追跡することは不可能だった。この問題を克服するため、研究グループは、筒状の半透膜を心臓の壁に埋め込み、この膜に透過して来る心筋間質の代謝物質を連続的に回収して測定する手法(マイクロダイアリシス法)を用いた。この方法を活用することで、従来の研究では達成し得なかった、虚血の前・虚血の最中・再灌流後の3つの時相のそれぞれについて、同一個体で連続的に心筋間質中の代謝物質を回収することに成功した。
その結果、心筋保護の鍵となる重要な因子であるグルタチオンという強力な還元物質が虚血および再灌流の時相で細胞外へ放出され、細胞内の活性酸素種を除去できなくなることを特定。さらにこの細胞外放出が、主にMRP1という特殊なトランスポーターを介していることを特定した。
MRP1阻害によるグルタチオン保持で、心筋細胞の生存を確認
活性酸素の増大は細胞内のさまざまな分子にダメージを及ぼすが、特に細胞膜のリン脂質が攻撃を受けやすいことが知られていた。特に近年では、細胞膜の脂質が過剰に酸化されると、膜としての構造を保てなくなり細胞全体が死に至ってしまうこと(フェロトーシス)も知られていた。その仕組みは盛んに研究されているものの、酸化した脂質はバリエーションに富んでおり構造的にも不安定のため解析が難しく、どのような酸化脂質が、いつ発生するのか、その詳細についてはこれまでわかっていなかった。
研究グループは、独自の手法を用いて詳細な酸化脂質種を解析。その結果、薬物によるMRP1の機能阻害で細胞内にグルタチオンを保持することは、活性酸素の消去のみならず、酸化脂質の減少を達成し、心筋細胞の生存を助けることを発見した。さらに、このようなフェロトーシスを標的にした治療法は、虚血再灌流後数時間後に開始しても一定の効果があることが示され、実際のヒトの治療法に応用可能なことがわかった。
MRP1阻害薬はヒトで安全に使用可能、臨床応用に期待
これまでも虚血再灌流障害に対して活性酸素を消去する薬剤の投与が試みられてきたが、その効果は限定的だった。この理由として考えられることの1つに、活性酸素が心筋梗塞のかなり早い段階から大量に発生するために、これ自体をターゲットとして薬剤を投与するのでは実際の病院の現場では手遅れであることが挙げられる。これに対し、今回心筋梗塞モデル動物で明らかにしたことは、心筋梗塞を発症してから6時間以降にみられる酸化脂質の増加をターゲットとすれば、治療薬投与までに時間的な猶予を生むことで効果的な治療ができるということだ。「MRP1阻害薬はヒトで安全に使用できることも過去の研究で確認されている。今後さらに詳細な病態の解析や遠隔期の効果を検証し、実用性を評価することで、心筋梗塞患者に、発病前と変わらない健康な未来をもたらすことを目指す」と、研究グループは述べている。
▼関連リンク
・慶應義塾大学 プレスリリース



