4種類のGタンパク質シグナルに分類されるGPCR、G12経路の研究は進んでいない
東北大学は8月21日、細胞における機能未解明の情報伝達経路であるG12シグナルを誘導できるデザイナーGタンパク質共役型受容体(デザイナーGPCR)を開発し、このデザイナーGPCRを脂肪細胞に発現する遺伝子組換えマウスを用いることで、通常はエネルギーを貯蓄するタイプの脂肪細胞(白色脂肪)からエネルギーを消費するタイプの脂肪細胞(褐色脂肪)への転換をG12シグナルが促進することがわかったと発表した。この研究は、同大大学院薬学研究科の井上飛鳥教授、小野雄基大学院生(研究当時)、医学系研究科の酒井寿郎教授、ドイツ・ハイデルベルク大学のRobert B.Russell教授らの研究グループによるもの。研究成果は、「Signal Transduction and Targeted Therapy」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
現在市販されている医薬品の有効成分は約1,400種類ある。そのうち、約3分の1がGタンパク質共役型受容体(GPCR)と呼ばれる膜タンパク質に作用するタイプの薬である。GPCRは細胞の表面に存在し、細胞外のホルモンなどを感知して細胞内に適切な情報(シグナル)を伝達するのが本来の機能である。多くの疾患は、シグナル伝達の異常が起因となるため、GPCR作用薬(シグナル誘導が作動薬、遮断は拮抗薬と呼ばれる)はこのような不適なシグナルを正常化することで細胞機能を戻して薬効を発揮する。
GPCRが伝達するシグナルは大きく4種類(Gs、Gi、Gq、G12)に分類され、GPCRごとに異なるシグナルを発する。これらのシグナルを担う因子は三量体Gタンパク質(以下、Gタンパク質)と呼ばれ、GPCRはそれぞれ好みのGタンパク質が異なると言える。このシグナルの視点から既存のGPCR作用薬を分類すると、3種類(Gs、Gi、Gq)のGタンパク質シグナル経路に関連するものがほとんどであり、G12シグナル経路に作用する薬は極めて少ない。この一因として、G12シグナルを解析する手法が限られ、G12シグナル型GPCRの研究が遅れているためと考えられる。
痩せ薬として期待されたGsシグナル型の作動薬は薬効不十分だった
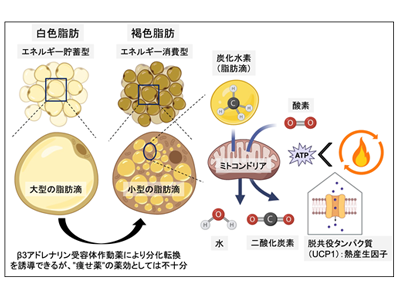
白色脂肪細胞はエネルギーを脂肪滴の形で貯蓄し、体のエネルギー状態が低下した時に脂肪滴からエネルギーを産生する。この仕組みはヒトの祖先が飢餓を生き抜く上では必須だったが、飽食の現代においては肥満を容易に引き起こし、これに起因するさまざまな疾患リスクにつながる。既存の抗肥満薬はいずれもエネルギー摂取を抑制する方向であり、すでに溜まっているエネルギーを消費する方向の薬はない。一方、脂肪細胞には、褐色脂肪細胞と呼ばれる熱産生能が高い細胞種が存在し、寒冷時などにおいて、白色脂肪細胞が褐色脂肪細胞へと分化転換する現象(脂肪細胞の褐色化)が知られている。β3アドレナリン受容体(β3AR、Gsシグナル型)に対する作動薬を投与すると、薬理的に褐色化を誘導することができることから、β3AR作動薬はエネルギー消費を高める薬、すなわち「痩せ薬」として期待されたことがあった。しかし、ヒトの臨床試験から薬効が不十分であることが報告され、β3AR作動薬は抗肥満薬としての開発は中断されている。
G12シグナル選択性高いGPCRを脂肪細胞に発現するマウス作出
研究グループは今回、G12シグナルを誘導するデザイナーGPCRの改良に取り組んだ。デザイナーGPCRはデザイナー薬との組み合わせで使われる化学遺伝学(ケモジェネティクス)の研究ツールである。以前の研究において、Gqシグナル型のデザイナーGPCRを改変することでG12シグナル型を開発し、この初期バージョンのデザイナーGPCRは他のGタンパク質にも弱いながらシグナル活性を示したことから、G12シグナルの選択性の向上を目指した。そこで、生物情報学解析を活用することで、選択性向上が期待される1アミノ酸変異を複数設計した。培養細胞を用いたシグナル計測により、G12シグナル選択性が改善したデザイナーGPCR(以下、G12D)を取得した。
次に、研究グループはこの新しいバージョンのデザイナーGPCRを特定の組織に発現させる遺伝子改変マウス(Stop-G12Dマウス)を作出した。特定の組織に発現させる手法として、Creリコンビナーゼを用いた手法が汎用されている。Stop-G12DマウスはデザイナーGPCRをどの組織でも発現しないが、特定の組織でCreリコンビナーゼを発現するマウスと交配させることで、その次の世代のマウスでは、Creリコンビナーゼが発現する組織でデザイナーGPCRが発現するようになる。この状態では、G12シグナルはまだ誘導されていないが、デザイナー薬をマウスに投与することでG12シグナルを特定の組織で誘導することができる。今回、研究グループはCreリコンビナーゼを脂肪細胞に発現するマウスにStop-G12Dマウスを交配させることで、脂肪細胞にデザイナーGPCRを発現させたマウス(脂肪G12Dマウス)を作出した。
遺伝子改変マウス、G12シグナルでβ3AR作動薬の効果高まり酸素消費量増加が持続
この脂肪G12DマウスとG12Dを発現しない対照群のマウスに対し、デザイナー薬を投与して脂肪細胞の形態や機能を調べたところ、両群のマウスで顕著な変化は認められなかった。そこで、脂肪細胞の褐色化を促す作用を有するβ3AR作動薬と共にデザイナー薬をこのマウスに投与した。その結果、β3AR作動薬の作用により両群のマウスで脂肪細胞の褐色化が生じていたが、その効果は脂肪G12Dマウスで顕著に高いことが、組織形態と遺伝子発現解析からわかった。
続いて、細胞レベルの褐色化がマウスの個体レベルでの代謝変化に影響を与えるか調べた。β3AR作動薬とデザイナー薬を前処置(褐色脂肪細胞を誘導)したマウスを代謝ケージに入れ、自由活動下での酸素消費量を計測した。その結果、両薬の追加投与により、両群のマウスで酸素消費量が増加したが(β3AR作動薬による効果)、脂肪G12Dマウスではこの酸素消費増加が持続していた。次に、両薬を前処置したマウスを寒冷ケージに入れ、体温変化を測定した。その結果、両群のマウスで徐々に体温が低下したが、脂肪G12Dマウスでは低下幅が小さいことがわかった。これらの結果から、脂肪G12Dマウスは褐色脂肪細胞が増加し、全身のエネルギー消費・熱産生が亢進することがわかった。
下流で働くシグナル経路も特定
最後に、培養細胞の実験により、脂肪細胞の褐色化の詳細な機構を調べた。薬物処置をしていないマウスの脂肪組織を摘出し、酵素処理により細胞を分散させ、脂肪細胞の前駆細胞を単離した。この細胞を適切な培地の中で培養することで、褐色脂肪細胞へと分化させた。この細胞にデザイナー薬を処置すると、褐色化が促進することが確認できた。この条件に対して、さまざまなシグナル伝達阻害剤を試したところ、デザイナー受容体の下流で働くシグナル経路を特定した。
以上の結果から、G12シグナルはGsシグナルによる脂肪細胞の褐色化を相乗的に促進することがわかった。この細胞種の転換により、個体レベルでエネルギー消費の亢進につながることが実証された。
エネルギー消費を亢進する肥満治療薬の創生が期待できる
今回の研究により、既存の痩せ薬であるエネルギー摂取を抑制するタイプとは異なる、エネルギー消費を亢進するタイプの肥満治療薬の創生が期待される。過去の研究では、β3AR作動薬をヒトに投与すると、褐色脂肪細胞の増加が生じるものの、痩せる効果は認められないという結果が報告されている。脂肪細胞にはG12シグナル型GPCRが多数発現しており、今後これらのGPCRに対する作動薬の開発が望まれる。この作動薬をミラベグロンなどのβ3AR作動薬と併用することで、エネルギー消費が大幅に亢進して痩せる効果が期待される。
「この研究で作出したG12シグナルのデザイナーGPCRとこれを発現させるStop-G12Dマウスは汎用性のある研究ツールである。別の種類のCreリコンビナーゼを使うことで、脂肪以外の組織にデザイナーGPCRを発現させて、G12シグナルの薬効を調べることができる。病態モデルマウスに対する治療効果が認められる場合、内在性に発現するG12シグナル型GPCRの作動薬の開発につながる。この方法論は一見回り道であるが、標的組織と特定のシグナルを介した薬効を調べるクリーンな手法であり、標的を絞って成功確率の高い治療薬を開発することに貢献する」と、研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース






