骨誘導因子BMPによる治療、FGF18との組み合わせが有望
東京医科歯科大学は8月9日、FGF18の新たな機能として、間葉系細胞のケモカインCCL2産生を促してM2マクロファージを誘導することで、骨修復を促進することをつきとめたと発表した。この研究は、同大大学院医歯学総合研究科分子発生学分野のNAMANGKALAKUL Worachat(ナマンカラクル ウォラチャット)大学院生(研究当時)、JIN Chengxue大学院生、吉本由紀講師、井関祥子教授、分子免疫学分野の永井重徳准教授、分子細胞機能学分野の中濵健一准教授、分子情報伝達学分野の中島友紀教授、東京理科大学、京都大学、順天堂大学らの研究グループによるもの。研究成果は、「Journal of Tissue Engineering」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
WntやNotchを初めとし、線維芽細胞増殖因子(FGF)や骨形成タンパク質(BMP)は、骨の発生やリモデリング、骨修復の過程で協調して機能する。特にBMP2は米国などで骨修復のためのゴールドスタンダードとされ、骨修復や骨増生における骨誘導因子として欠かせない。しかし、BMP2だけで治療するには高容量を必要とし、また術後炎症などの副作用を引き起こす心配があるため、他の因子を組み合わせるなどの必要性が考えられる。その候補として、FGFファミリーに属し、骨形成の正の制御因子として同定されたFGF18がある。研究グループはこれまでに、FGF18がBMP2の骨修復作用を増強することを示したが、その詳細なメカニズムは、いまだにわかっていなかった。
近年、炎症およびマクロファージ活性化の制御におけるFGFシグナル伝達経路の関与が明らかになりつつある。マクロファージは、病原体を駆除し、組織の治癒を促進するために炎症のさまざまな局面に関与する免疫細胞である。さらには、骨を含む多くの組織において、組織修復、組織再生、恒常性の維持、免疫監視にも関わっている。マクロファージには、極性を持たないM0マクロファージのほか、機能面から大きくM1マクロファージとM2マクロファージに大別されるが、特にM2マクロファージは炎症反応を抑える以外に、治癒を促進したり、修復を促したりする性質があることから、FGF18の骨修復作用がM2マクロファージを介する可能性があると考えた。
マウス骨欠損部、FGF18+BMP2治療でM2マクロファージ関連遺伝子発現
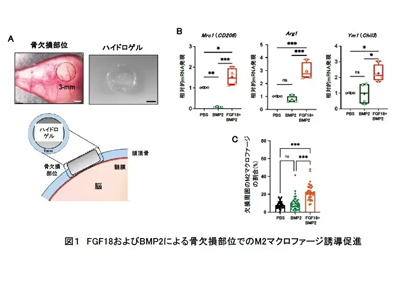
臨界サイズのマウス頭蓋冠欠損モデルで、BMP2依存性の骨修復において、FGF18がBMP2の機能を増強するかを調べるため、これらの因子を含んだコレステリル基とアクリロイル基を有するプルラン(CHPOA)ナノ架橋(NanoClik)ハイドロゲルを4週齢のマウスの骨欠損部に埋め込んだ。手術5日後に欠損部の骨縁と硬膜を回収して遺伝子発現を調べたところ、M2マクロファージ関連遺伝子(CD206、Arg1、Ym1など)の発現が、FGF18+BMP2群のみで上昇していた。実際に、術後7日目の組織において、FGF18+BMP2群でM2マクロファージの浸潤が、他の群に比べて有意に増加していた。
次に、本当にマクロファージが関与しているかを確かめるために、クロドロン酸リポソームを投与して、1週間あるいは2週間マウス体内のマクロファージを除去し、頭蓋冠欠損モデルで骨修復の度合いを比較したところ、マクロファージ除去期間が長いほど、FGF18+BMP2群での骨修復が抑制された。また、術後4週間後において、BMP2群とFGF18+BMP2群の差がなくなったことから、FGF18による骨修復には、M2マクロファージが関与している可能性が示された。
FGF18、BMSCに作用し間接的にM2マクロファージ誘導促進
そこで、M2マクロファージ誘導へのFGF18の関与について骨髄細胞を用いて検討した。骨髄細胞は、白血球(免疫系細胞)とそれらを支持する間葉系の骨髄間質細胞(bone marrow stroma cell;BMSC)から構成される。マウス骨髄細胞を取り出し、免疫系細胞を分離してM-CSF含有培地で7日間培養すると、マクロファージの元となる細胞(前駆細胞)からM0マクロファージに分化するが、この時IL-4を添加すると極性が変化してM2マクロファージが誘導される。そこでIL-4の代わりにFGF18を添加したが、M2マクロファージは誘導されず、FGF18は直接M2マクロファージを誘導しないことがわかった。一方、取り出した骨髄細胞を、FGF18を添加して培養するとM2マクロファージが誘導された。そこで、骨髄細胞からBMSCを分離して、FGF18を添加して72時間培養し、上清培地(BM-CM)を得た。このBM-CMでM0マクロファージを培養したところ、M2マクロファージ関連遺伝子発現の上昇とともに、M2マクロファージが誘導された。すなわち、FGF18がBMSCに作用して発現する因子が、間接的にM2マクロファージへの誘導を促進することがわかった。
CCL2/CCR2を介してM2マクロファージ誘導
このBMSCから分泌される因子を同定するために、FGF18処理したBMSCからRNAを抽出して、マイクロアレイ法によって網羅的に遺伝子発現を解析し、発現上昇した遺伝子群から候補因子を探索した。その中で、マクロファージの活性化や骨形成、骨修復時の炎症に関わるCCケモカインリガンド2(CC chemokine ligand 2;CCL2)に着目した。M0マクロファージの培養にCCL2を添加すると、M2マクロファージ関連遺伝子の発現が上昇した。逆に、抗CCL2中和抗体で前処理してBM-CM中のCCL2の活性をなくすと、BM-CMによるM2マクロファージ関連遺伝子の発現が低下することから、CCL2がFGF18によるM2マクロファージ誘導に関与することが示された。
最後に、骨修復にCCL2が実際に関わっているかをマウスで確かめるため、CCL2の受容体であるCCR2(CC chemokine receptor 2;CCR2)を欠損するマウスで、頭蓋冠欠損修復実験を行った。すると、FGF18+BMP2群において、野生型マウスに比べて治癒率が低かったことから、 FGF18による骨修復促進作用の一部は、CCL2/CCR2シグナルを介していることが示された。
頭蓋顔面骨欠損の新規治療法開発への応用が期待できる
研究グループは、FGF18によるBMSCの刺激が、CCL2を含むケモカインの発現上昇を引き起こし、M2マクロファージへの誘導過程に寄与することを明らかにした。FGF18添加による骨修復は、質と量ともにBMP2単独投与よりも利点があることが以前の研究で示されており、これがマクロファージ活性化の制御によるものであることが示唆された。したがって、「今回得られた知見は、骨組織工学においてFGF18の補助的利用の可能性を広げるものであり、頭蓋顔面骨欠損の治療として、臨床における新規戦略の開発に有望と考えられる」と、研究グループは述べている。
▼関連リンク
・東京医科歯科大学 プレスリリース




