iMSCから高品質な軟骨スフェロイドを作製するには?
京都大学iPS細胞研究所(CiRA)は6月8日、iPS細胞由来の間葉系幹細胞から、関節軟骨修復に適した軟骨スフェロイドを作製する方法を確立したと発表した。この研究は、CiRA臨床応用研究部門のDenise Zujur研究員、池谷真准教授らの研究グループと、佐賀大学医学部 附属再生医学研究センターの中山功一教授、味の素株式会社ほかとの共同研究によるもの。研究成果は、「Frontiers in Cell and Developmental Biology」に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
軟骨は、関節を滑らかに動かす役割をする組織だが、血管を持たないため、細胞の増殖や分化を促進するために必要な物質の供給が不十分だ。そのため、一旦損傷すると修復が難しく、関節痛や変形などの原因となることがある。
現在は再生医療として、患者自身の体から取り出した軟骨細胞や間葉系幹細胞を培養し、軟骨へと分化させて移植する取り組みがある。しかし、この手法では細胞提供者に由来する合併症、限られた増殖能、脱分化などの課題があった。iPS細胞は体の外で大量に培養することができるため、細胞治療用の軟骨を大量に作るための材料の一つとして期待されている。また、血液の細胞からつくることができ、あらかじめ作製し保存されているiPS細胞も利用することができるため、細胞採取の際に患者にかける負担が少ない。
これまで研究グループは、iPS細胞から神経堤細胞を経由して間葉系幹細胞(iMSC)を作製し、得られたiMSCがさまざまな細胞に分化すること、創薬や疾患モデリングに利用できることを示してきた。また、再生医療用の細胞を作製するために、動物由来成分を含まない方法でiMSCを培養する方法を確立してきた。今回は、軟骨への分化を促進する低分子化合物として「TD-198946」を用いて、iMSCから高品質な軟骨の塊(スフェロイド)を作製することを目指して研究を行った。
段階的に分化させて作られた軟骨スフェロイドは、従来のものと比べて高品質
まず、iMSCから軟骨様組織を作るための効率的な分化方法を確立するため、異なる条件で作られた複数のiMSC(T1-iMSCおよびXSF-iMSC)と骨髄由来MSC(BM-MSC)を比較検討した。その結果、T1-iMSCは他と比べて軟骨形成に優れていると同時に、骨や脂肪は形成しにくいことが明らかになった。
MSCの軟骨分化は、従来TGF-βや骨形成タンパク質(BMP)などの因子で持続的に刺激することで行われてきた。近年は段階的に分化させる方法が登場している。そこで、TGF-βとBMPに加え、軟骨形成を促進する低分子化合物であるTD-198946(TD)を使用し、軟骨スフェロイドを作る方法として、従来の方法と三段階誘導法とを比較した。その結果、段階的に分化させて作られた軟骨スフェロイドは従来法のものと比較して、高品質(関節軟骨マーカーであるRPG4の発現が高く肥大軟骨マーカーであるCOL10A1の発現が低い)であることが判明した。
移植しても脱分化や線維性軟骨形成などの兆候はなく、生体内で軟骨が維持
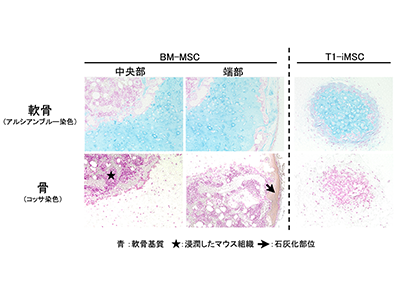
さらに、軟骨スフェロイドを生体内に移植した際に、その性質が維持されるか確かめた。T1-iMSCあるいはBM-MSCから作製した軟骨スフェロイドを免疫不全マウスの皮下に移植。8週間後に移植したスフェロイドを採取し、顕微鏡で観察した。
その結果、BM-MSCから作製した軟骨スフェロイドには、8週間後には軟骨様組織の他に石灰化し、骨様組織ができ始めていた。一方、T1-iMSCから作製した軟骨スフェロイドは、8週間後でも軟骨として残っていた。また、段階的に分化させる方法で作られた軟骨スフェロイドは近くに存在していると接着し、7日目には完全に融合していたという。
軟骨スフェロイドは数日程度で融合するため、より大きな軟骨組織の構築も可能
今回の研究により、軟骨を修復・再生する能力をもつ軟骨前駆細胞をiMSCから製造する方法が開発された。この方法により、軟骨前駆細胞を安定的に大量に製造することができると考えられる。
「本成果は幹細胞を使った軟骨修復の新しい細胞源として、iMSCが利用可能であることを示している。さらに、軟骨スフェロイドは数日程度で融合するため、剣山メソッド型のバイオプリンターなどを利用して、より大きな軟骨組織を構築することもできると考えられる」と、研究グループは述べている。
▼関連リンク
・京都大学iPS細胞研究所(CiRA) ニュース



