神経膠腫の中で、最も頻度が高く予後も悪い膠芽腫、再発後の1年生存割合は14%
東京大学医科学研究所は7月22日、口唇ヘルペスのウイルスである単純ヘルペスウイルス1型に、人工的に3つのウイルス遺伝子を改変した第三世代のがん治療用ヘルペスウイルス G47Δの臨床開発を進めており、悪性神経膠腫に対するG47Δの製造販売承認申請の主試験となった、悪性度が最も高い神経膠腫である膠芽腫の患者を対象に実施した医師主導治験(第II相臨床試験)の最終解析結果を報告したと発表した。この研究は、同研究所附属病院脳腫瘍外科(同研究所附属先端医療研究センター先端がん治療分野)の藤堂具紀教授らの研究グループによるもの。研究成果は「Nature Medicine」にオンライン掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
神経膠腫(グリオーマ)は、原発性脳腫瘍のおよそ4分の1を占め、代表的な悪性脳腫瘍である。神経膠腫は悪性度に従って4段階に分けられ、悪性度の高い2つの段階のもの(悪性度3と4)を悪性神経膠腫と呼ぶ。治験の対象となった膠芽腫(グリオブラストーマ)は、最も頻度が高く予後も悪い悪性度4の神経膠腫である。初発膠芽腫に対して、放射線治療と化学療法(テモゾロミド)に交流電場腫瘍治療システムを併用した米国の最近の報告でも、その全生存期間中央値は診断から20.9か月とされる。再発は必至であるが、再発後に有効な治療法は未だに確立されておらず、膠芽腫の再発後の1年生存割合は14%と報告されている。
単純ヘルペスウイルス1型の3つのウイルス遺伝子を改変し、新しいがん治療に
がんのウイルス療法とは、がん細胞のみで増えることができるウイルスを感染させ、ウイルスが直接がん細胞を破壊する新しい治療法である。ウイルス療法では、遺伝子工学技術を用いてウイルスゲノムを設計して、がん細胞ではよく増えても正常細胞では全く増えないウイルスを人工的に造って臨床に応用する。G47Δは、口唇ヘルペスの原因ウイルスとして知られている単純ヘルペスウイルス1型の3つのウイルス遺伝子を改変した世界初の第三世代のがん治療用ヘルペスウイルスである。
13例を対象としたFIH試験で、直接的殺細胞作用、特異的抗腫瘍免疫作用、安全性を確認
ファースト・イン・ヒューマン試験(FIH試験)は、2009年から2014年まで、東京大学医学部附属病院と東京大学医科学研究所附属病院で第1/2相臨床試験として実施された。進行性の膠芽腫患者13例を対象とし、2段階で用量の増加を行った。定位脳手術で腫瘍内の同じ座標に2週間以内に2回の投与を行い、G47Δの安全性を確認した。G47Δの副作用は主として免疫反応に伴うものだった。生検組織の解析では、G47Δ投与後短期間のうちに、腫瘍細胞に向けたリンパ球の浸潤が生じることが観察された。そのため、G47Δ投与直後より、MR画像上、腫瘍全体が膨らむ所見が見られた。この所見は、医師主導治験(第2相臨床試験)において、ウイルス療法に特化した腫瘍縮小効果判定基準を導入する根拠となった。
G47Δは、即時効果として腫瘍細胞に対する直接的殺細胞作用、遅発効果として特異的抗腫瘍免疫作用の2段階で抗腫瘍作用を現すことが示された。今回のFIH試験により、G47Δの腫瘍内への繰り返し投与の安全性が確認され、第2相臨床試験で用いる投与量の設定根拠が示された。被験者13例のうち3例が長期生存(46か月以上)し、うち1例は現時点でG47Δ治療後の再発なく12年以上生存している。また長期生存例に遅発性の副作用は見られなかった。
残存または再発したテント上膠芽腫患者の医師主導治験では、最大6回の投与で1年生存割合84.2%
医師主導治験は、東京大学医科学研究所附属病院の単施設で実施された単アームの治験(第2相臨床試験)である。放射線療法およびテモゾロミド投与後に腫瘍が残存または再発したテント上膠芽腫患者を対象にし、2015年から2018年まで被験者登録が行われ19例が治験に参加した。G47Δは定位脳手術によって腫瘍内に、最大6回まで繰り返し投与された。治験実施計画に従い、治療開始から1年経過した患者13名で中間解析を実施したところ、主要評価項目であるG47Δ治療開始後の1年生存割合が事前に設定されていた有効性の基準を越えたため、本治験は早期終了(有効中止)となった。
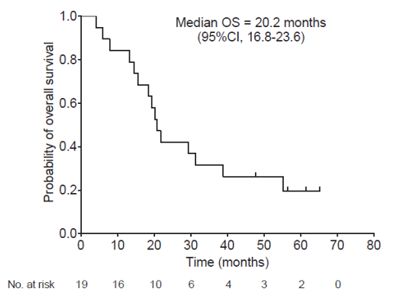
19例の最終解析の結果、G47Δ治療開始後の1年生存割合は84.2%(95%信頼区間 60.4-96.6%、以下同様)だった。副次評価項目については、G47Δ治療開始後の全生存期間中央値が20.2か月(16.8-23.6か月)、初回手術からの全生存期間中央値が28.8か月(20.1-37.5か月)、G47Δ治療開始後の無増悪生存期間中央値が4.7か月(3.3-6.1か月)となった。G47Δと関連する有害事象は、発熱(17/19、89.5%)が最も頻度が高く、続いて嘔吐、悪心、リンパ球減少、白血球減少だった。MR画像上の特徴として、G47Δ投与直後に、投与部位に一致して腫瘍内部が抜けて見える所見(造影効果の消失)と、腫瘍全体が膨らむ所見(造影領域の拡大)が、G47Δ投与の度に繰り返し認められた。
従来の治療とは異なり、治療効果が腫瘍縮小に反映されない
従来の治療とは異なり、生存期間延長などの治療効果が、MR画像上の腫瘍縮小に反映されないことがG47Δによるウイルス療法の特徴であることが示された。従って、G47Δ治療開始から最終投与後24か月までのMR画像上の最良効果は、PR(部分奏功)が1例(5.3%)、SD(安定)が18例(94.7%)だった。生検組織の解析から、MR画像で腫瘍内部が抜けた部分は、ウイルス複製に伴う腫瘍細胞の破壊を反映しており、腫瘍全体の拡大はリンパ球の腫瘍内への浸潤を反映していること(immunoprogression)が示された。更に、腫瘍内に浸潤するCD4陽性Tリンパ球、CD8陽性Tリンパ球の数がG47Δの投与の度に顕著に増加して、G47Δ治療後も長期間増加した状態が続くこと、一方で制御性T細胞の数は低く保たれることが観察された。
腫瘍内に浸潤したTリンパ球は、腫瘍細胞を認識して腫瘍の増大を抑制している可能性があるものの、抗腫瘍免疫が腫瘍の縮小を引き起こすまでには、G47Δ治療開始後4~5か月以上かかることがわかった。現時点で19例のうち3例が、G47Δ治療後の再発なく4年以上生存しているという。
2021 年6月日本初のウイルス療法薬として承認、脳腫瘍以外のがんへの適応拡大に期待
G47Δは、今回の治験を主試験として製造販売承認申請がなされ、2021 年6月に日本初のウイルス療法薬(再生医療等製品、一般名テセルパツレブ、製品名デリタクト注)として承認(条件及び期限付承認)された。脳腫瘍に対しては世界で初めて承認されたウイルス療法薬である。2021年11月より悪性神経膠腫を適応症として販売が開始されている。G47Δの長期効果には抗腫瘍免疫が関与し、それが腫瘍縮小を来すにはG47Δ治療開始後4~5か月以上要することを考慮すると、初期治療後なるべく早い時期にG47Δの治療を行う方が効果的であると考えられる。「G47Δは全ての固形がんに同じメカニズムで同じく作用することから、今後脳腫瘍以外のがんにも適応が拡がることが期待される」と、研究グループは述べている。
▼関連リンク
・東京大学医科学研究所 プレスリリース






