免疫細胞の活性化や炎症を抑える分子「レグネース-1」に着目
日本医療研究開発機構は5月12日、免疫細胞の活性化や炎症を抑えるブレーキとしての働きをもつRegnase-1(レグネース-1)の働きを増強することで、免疫細胞の活性化を抑え、急性呼吸促拍症候群や、肺線維症、多発性硬化症モデルマウスの病状を改善する方法の開発に成功したと発表した。この研究は、京都大学大学院医学研究科の竹内理教授らの研究グループによるもの。研究成果は、「Science Translational Medicine」にオンライン掲載されている。
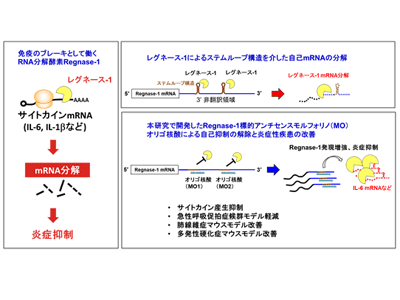
画像はリリースより
(詳細は▼関連リンクからご確認ください)
マクロファージやT細胞などの免疫細胞は、細菌やウイルスなどの病原体感染時に活性化し、サイトカインなどのタンパク質を作り細胞外に分泌して炎症を起こす。適度な炎症や免疫細胞活性化は感染した病原体の排除に重要だが、過剰な活性化や慢性化、また自分自身に対する免疫応答は、さまざまな炎症性疾患の発症につながる。例えば、細菌やウイルスの呼吸器感染による急性呼吸促拍症候群(ARDS)に、免疫応答の過剰な活性化やサイトカイン産生(サイトカインストームとも呼ばれる)が関わることは、新型コロナウイルス感染症の重症化機序の研究からも明らかにされている。また、慢性的な炎症は、特発性肺線維症や肝硬変など、臓器の線維化による疾患の原因ともなっている。免疫系が自分自身を攻撃してしまういわゆる自己免疫疾患にも炎症が深く関与している。ヒトの自己免疫疾患には、慢性関節リウマチや、多発性硬化症、潰瘍性大腸炎など多くのものが知られている。ARDSや特発性肺線維症に対する有効な治療法は限られており、自己免疫疾患に対しては、免疫抑制剤や生物学的製剤が用いられ急速に治療法が進歩しているが、いまだにこれらの治療法に不応性の患者も存在している。新たな炎症制御法の開発は、炎症の関連するさまざまな疾患に効果を示す可能性がある。
マクロファージにおけるサイトカイン産生は、その細胞に存在するトル様受容体(TLR)をはじめとした病原体センサーにより病原体の感染を検知し、そのシグナルを核に伝えるところから始まる。核の中でDNAから、サイトカインなど免疫応答に関わるタンパク質をコードするメッセンジャーRNA(mRNA)が転写され、細胞質へ移動し、タンパク質へと翻訳され、働く。T細胞など他の免疫細胞でも病原体の抗原を認識すると、同様の機構で活性化し、免疫応答をコーディネートしている。
免疫細胞の活性化は、普段は緻密に制御され、過剰な活性化を防いでいる。この免疫応答の抑制機構の一つとして、サイトカインなど免疫応答の関わるタンパク質をコードするmRNAの量の調節がある。中でも、研究グループがこれまで研究を行ってきたレグネース-1は、インターロイキン6(Interleukin-6、IL-6)などのサイトカインはじめとした免疫細胞活性化に関連するタンパク質をコードするmRNAを分解しその量を減らすRNA分解する酵素として機能し、免疫応答のブレーキとして働くタンパク質。レグネース-1は、mRNAの3’非翻訳領域に存在するステムループ構造を認識して結合し、分解することで翻訳されるサイトカインなど免疫応答に関わるタンパク質の量を調節している。マウスでレグネース-1を欠失させると、免疫系の暴走が起こり、自己免疫性炎症性疾患を発症するが、近年の研究で、ヒト潰瘍性大腸炎の上皮でレグネース-1の機能獲得変異が見つかったり、特発性肺線維症患で、その病理に関わる2型自然リンパ球(ILC2)細胞において細胞数とレグネース-1発現に負の相関を認め、マウスにおいてILC2の制御にレグネース-1が重要であることが明らかとなっている。
したがって、レグネース-1は、抗サイトカイン治療や免疫抑制剤とは異なる、炎症性疾患の新たな疾患治療標的となると考えられる。しかし、これまでレグネース-1を調節する制御法は開発されていなかった。
レグネース-1の自己分解を阻害するアンチセンスオリゴで発現量増加に成功
今回の研究では、レグネース-1の働きを高めることにより、免疫応答・炎症のブレーキを強める手法の開発に取り組んだ。そのために、もともと存在するレグネース-1発現の制御メカニズムを利用した。レグネース-1タンパク質もmRNAから翻訳されて作られるが、レグネース-1をコードするmRNA自身がステムループ構造を持ち、レグネース-1により分解されることを見出していた。つまり、レグネース-1によって自身のmRNAおよびタンパク質の量が制御されており、レグネース-1のタンパク質やmRNAの変化に対して、その量を最終的に元に戻すような役割を果たしていると考えられる。
まず、レグネース-1 mRNAの3’非翻訳領域を詳細に解析したところ、自分自身により認識される2か所のステムループ構造をとる配列が明らかとなり、それがヒトやマウスを始め多くの生物種で類似していることがわかった。そこで、このステムループ構造を壊すことで、レグネース-1タンパク質によるレグネース-1 mRNAの分解を阻害し、増加したmRNAから多くのレグネース-1タンパク質を作らせることを目的とした検討を行った。
レグネース-1のmRNAに存在するステムループ構造を特異的に破壊するために、この構造をとる2か所のRNA配列に相補的に結合するようなオリゴ核酸をそれぞれ設計した。このオリゴ核酸が細胞内でレグネース-1 mRNAに相補的に結合することにより、ステムループ構造をとることができなくなり、レグネース-1による自己抑制が解除されることが期待された。核酸のバックボーンとしては、これまで核酸医薬として臨床応用もされているモルフォリノオリゴ修飾核酸(以下、MO核酸)を用いて合成した。このレグネース-1標的MO核酸を細胞に導入すると、レグネース-1タンパク質がレグネース-1 mRNAに結合し分解するのを抑制し、レグネース-1のmRNAやタンパク質量が増加する事を確認した。
レグネース-1標的MO核酸はARDS、肺線維症、EAEマウスの病態を改善
レグネース-1標的MO核酸は、マウスマクロファージに導入すると、レグネース-1の発現を増強し、これに反比例して、TLR刺激に対するIL-6などの炎症性サイトカイン産生を抑制した。これに対し、I型インターフェロンなど核酸による副作用と考えられる遺伝子発現には影響を与えなかった。また、ヘルパーT細胞に導入した際も、感染に対する応答に加えて自己免疫疾患にも関わるTh1やTh17細胞分化を抑制した。すなわち、レグネース-1標的MO核酸は細胞レベルで、レグネース-1の発現を増加させ、免疫細胞活性化のブレーキ能を高めることに成功したと考えられた。
次に、マウスを用いて個体レベルでレグネース-1標的MO核酸の炎症性疾患に対する有効性を検証。その際には、組織導入性を高めたvivoモルフォリノオリゴ核酸を用いた。まず、急性炎症モデルとして、TLR4を刺激する細菌成分であるリポポリサッカライド(LPS)による急性呼吸促拍症候群(ARDS)にレグネース-1標的MO核酸を経気道的に前処置したところ、肺での炎症性サイトカイン発現や免疫細胞浸潤を有意に抑制し、肺障害も改善することがわかた。次いで、肺線維症のマウスモデルに対するレグネース-1標的MO核酸の効果を検討した。MO核酸の経気道投与により、炎症が引き金となって誘発される肺の線維化に関わるコラーゲンなどの遺伝子発現や肺への免疫細胞浸潤、肺の線維化の改善を認めた。したがって、レグネース-1標的MO核酸の経気道投与は、肺における急性、慢性炎症性疾患の軽減に効果を示した。
レグネース-1はさまざまな自己免疫疾患と関連する事から、自己免疫疾患マウスモデルに対するレグネース-1標的MO核酸の効果検証も試みた。これまでに、多発性硬化症のマウスモデルである実験的自己免疫性脳脊髄炎(EAE)へのレグネース-1の関与が報告されており、研究グループもレグネース-1のヘテロ欠損によりEAEが増悪することを見出した。そこで野生型マウスにEAEを発症させ、レグネース-1標的MO核酸を疾患発症前に脳室内投与した。その結果、麻痺などの臨床症状や脊髄への免疫細胞浸潤が有意に改善し、脊髄でのサイトカイン発現の抑制を認めた。また、発症後の脊髄免疫細胞の1細胞シークエンス解析の結果、神経系のマクロファージ様細胞であるマイクログリア細胞が炎症抑制型に変化していることが明らかとなった。すなわち、レグネース-1標的MO核酸は、自己免疫疾患の改善にも効果を示すことが考えられた。
ヒトでレグネース-1と多発性硬化症との関連を確認
最後に、ヒト多発性硬化症とレグネース-1の発現に関して検討を加えた。その結果、レグネース-1 mRNAの血液細胞における発現とMRI検査で認められる多発性硬化症患者の病変部位の大きさに逆相関があることがわかった。
ヒト用に設計したMO核酸で、ヒト免疫細胞のサイトカイン産生抑制も確認
ヒトレグネース-1の3’非翻訳領域に存在するステムループ構造を標的としたアンチセンスMO核酸を合成して行った検討では、このMO核酸がヒトマクロファージ細胞株や血液由来単球においても、レグネース-1の発現を増強させ、LPS刺激によるサイトカイン産生を抑制する機能を発揮することも示した。
今回の研究で、レグネース-1の自己制御を標的としたアンチセンスMO核酸が、レグネース-1の発現と免疫応答のブレーキ機能を増強し、これにより、さまざまな炎症性疾患を軽減することを見出した。この研究では主にマウスを用いて検証したが、ヒト細胞でもヒト用に設計したレグネース-1標的MO核酸が効果を示している。将来的には、難治性の炎症性疾患の治療に発展させていく事を研究グループは視野に入れており、そのためには、オリゴ核酸の最適化やドラッグデリバリーシステムの構築など越えなければならないハードルは多く存在するため、今後、さらに研究開発を続けていきたいとの考えを示している。
▼関連リンク
・日本医療研究開発機構 プレスリリース



