膵がんの新たな腫瘍マーカーとしてマイクロバイオームが利用可能かを検証
東京医科大学は4月19日、マイクロバイオームをマーカーとして膵がんの早期発見や抗がん剤の治療効果予測に利用できる可能性が明らかになったと発表した。この研究は、同大消化器内視鏡学分野の永田尚義准教授、国立国際医療研究センター消化器内科の小島康志医長、久田裕也医師、忌部航医師(現:小田内科院長)、糖尿病研究センターの植木浩二郎センター長、感染症制御研究部の秋山徹室長、欧州分子生物学研究所の西嶋傑氏、Peer Bork氏らの研究グループによるもの。研究成果は「Gastroenterology」オンライン版に掲載されている。
画像はリリースより
(詳細は▼関連リンクからご確認ください)
膵がんは最も致死率の高い悪性腫瘍の一つであり、その罹患率は世界的に増加している。膵がんの原因解明や早期発見に有用な非侵襲的腫瘍マーカーの同定は喫緊の課題だ。人体には数百兆個・千種類以上の常在菌が消化管に生息しており、それら常在菌やウイルス(ファージ)の集合は総じて「マイクロバイオーム」と呼称され、ヒトの健康と病気を理解する上での重要な要素となっている。
研究グループは、最新の解析技術を用いて口腔内や腸内の微生物遺伝子を網羅的に検出することを試み、マイクロバイオームが膵がんの新たな腫瘍マーカーとして利用できる可能性を検証。また、世界で利用できる腫瘍マーカー同定のために、ドイツ人とスペイン人の口腔・腸内マイクロバイオームも調べ、日本人の結果と比較した。近年、動物実験から特定の腸内細菌種の存在が抗がん剤の効果を決定することがわかっているが、ヒトでは十分な研究が行われていなかった。そこで、膵がん患者において、マイクロバイオームが抗がん剤効果の予測に有用かも検証した。
膵がんに特徴的な口腔内細菌種と腸内細菌種を発見
日本人の膵がん患者と、年齢、性別、患者背景因子を1:5でマッチしたコントロール症例について、唾液と糞便をショットガンメタゲノムシークエンスで解析した。その結果、口腔細菌517種と腸内細菌1,151種を同定し、コントロール症例と比較することで膵がん患者に特徴的な口腔細菌18種と腸内細菌30種を発見した。
また、重要なこととして、日本で同定した膵がん関連腸内細菌が、ドイツ人やスペイン人の膵がん関連細菌と一致することを見出した。ヨーロッパ・日本の共通菌5種のうち、膵がんで増加した4種は、通常は腸内ではまれな口腔の常在菌であること、一方、減少した1種は多くの病気でも減少が報告されており、免疫誘導と関わる菌であることがわかっている。さらに、膵がん患者で3か国に共通して増加していた4種を宿主とする新規バクテリオファージ58種を発見した。
これらの結果は、特定の細菌の増加または減少が膵がんの発生やがん進行の原因となる可能性を示唆しており、今後それらの細菌を介した発がん機構の解明が望まれる。また、それら細菌が実際に発がんや進行の原因である場合は、それらをターゲットとするファージセラピーにより膵がんを予防または治療できる可能性があり、研究結果はその基盤データを提供したことになる。
IPMNや慢性膵炎に関連する腸内細菌種が、膵がん関連菌種と類似
次に、膵がんで認めた特徴的な腸内細菌叢が、膵がんリスク患者群のものと類似しているのかを検証したところ、膵管内乳頭粘液性腫瘍(IPMN)や慢性膵炎の腸内細菌叢は膵がん患者のものと類似することを見出した。また、慢性膵炎患者(相関係数0.63)の腸内細菌叢の方がIPMN患者(相関係数0.54)のものよりも膵がん患者の腸内細菌叢と類似していることもわかった。
他の病気についても同様の解析を行い、膵がん患者に特徴的な腸内細菌叢は、糖尿病、炎症性腸疾患、大腸がんの腸内細菌叢とは異なっており区別できるものの、胃酸分泌抑制薬であるProton-pump inhibitor(PPI)使用者の腸内細菌叢とは類似していることがわかった。疫学研究で、IPMN、慢性膵炎、PPI使用は膵がんリスクと関連することが報告されており、研究結果は、腸内細菌叢がこれらの病態と膵がんとを結びつける一つの要因であることを示唆した。
膵がん予測に口腔および腸内細菌種は有用、血液マーカーとの併用で予測精度向上
膵がんに特徴的な細菌叢が「がんの早期発見」のための腫瘍マーカーとして利用できるかを検証した。口腔と腸内細菌叢の膨大な情報から機械学習法という解析法を用いて膵がんの予測能を調べたところ、特定の口腔や腸内細菌を数菌種用いると高い確率で膵がんを予測できることがわかった。さらに、従来の血液マーカー(例:CA19-9)と口腔や腸内細菌種を併用すると、血液マーカー単独よりも膵がんの予測精度が高まることを発見した。
抗がん剤投与後の予後に腸内細菌種が関連することを発見
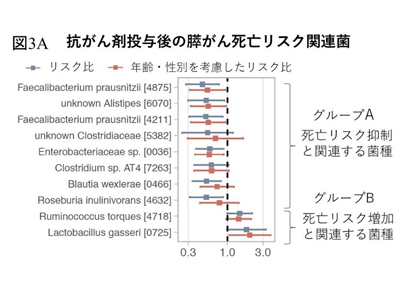
研究グループは、腸内細菌叢を「膵がん発見のマーカー」としてだけなく、「膵がん診断後の治療効果予測」にも利用できるのではないかと考えた。そこで、治療前に採取した糞便の腸内細菌と抗がん剤治療後の死亡率との関連を調べた。まず、腸内細菌叢を用いた死亡予測モデルを作成することで、膵がん患者を死亡リスクが低い腸内細菌叢グループAとリスクが高いグループBに分けた。死亡リスクが低いグループAに豊富に見られる菌種の多くは酪酸や酢酸など短鎖脂肪酸を産生する菌と判明。実際、グループAの菌種を有する患者は、グループBを有する患者と比較して、有意に抗がん剤治療後の生存率が長いことを見出した。短鎖脂肪酸には免疫の恒常性を保つ働きがあることが分かっており、グループAの菌種の存在が宿主の免疫応答を調整することで予後良好な結果になっている可能性が示唆された。
膵がん診療における個別化医療の実現に期待
今回の研究から、マイクロバイオームをマーカーとして膵がんの早期発見や抗がん剤の治療効果予測に利用できる可能性が明らかとなり、膵がんや予後のハイリスク患者の絞り込みから膵がん診療における個別化医療の実現が期待される。また、従来の血液腫瘍マーカーと唾液や糞便マーカーと組み合わせることで、より早期の膵がん発見が可能となり、治療率向上と予後改善が期待される。「膵がんに特異的な腸内細菌に感染するバクテリオファージの同定は、がんの発生や進行を抑制することを目指したファージセラピーの研究開発を促進させる」と研究グループは述べている。
▼関連リンク
・東京医科大学 プレスリリース






