次世代ICI標的分子として注目のLAG-3、TIM-3、TIGIT
慶應義塾大学は9月21日、次世代免疫チェックポイント阻害剤の標的分子であるLAG-3、TIM-3、TIGITを用いた腎細胞がんの新規分類を開発したと発表した。この研究は、同大医学部泌尿器科学教室の髙松公晴共同研究員、田中伸之専任講師、大家基嗣教授、腫瘍センターゲノム医療ユニットの西原広史教授らの研究グループによるもの。研究成果は、「Nature Communications」のオンライン版に掲載されている。
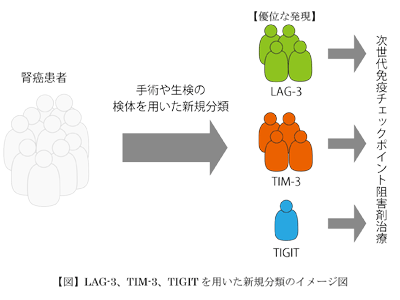
画像はリリースより
通常、体内ではリンパ球などの免疫細胞ががん細胞を異物として認識し、攻撃することでがん細胞を排除している。しかし、がん細胞は免疫チェックポイント分子と呼ばれるタンパク質を発現することでリンパ球の攻撃から逃れている(がん免疫逃避機構)。免疫チェックポイント分子としてPD-1やCTLA-4が同定され、がん免疫逃避機構をブロックする免疫チェックポイント阻害剤としてPD-1/PD-L1阻害剤やCTLA-4阻害剤が開発された。
これらの薬剤は多くのがんで使用されているが、一部の症例では効果が弱いことが問題となっている。がん微小環境の理解が進むにつれ、がん細胞が複数の免疫チェックポイント分子を用いて免疫から逃避していることが明らかになった。現在、次世代の免疫チェックポイント分子を標的とした新規抗がん剤の開発が行われており、LAG-3、TIM-3、TIGITは有望な標的分子として注目されている。
3分子の発現解析で腎細胞がん症例を分類、LAG-3発現優位は予後不良
今回、研究グループは淡明細胞型腎がん組織におけるLAG-3、TIM-3、TIGITの発現強度を単一細胞ごとに評価することにより、腎細胞がんの新規分類を作成した。また、3分子を同時染色するとLAG-3、TIM-3、TIGITの発現が相互排他性を有する傾向が明らかになった。新規分類におけるがん微小環境を評価すると、LAG-3発現が優位な症例ではがん免疫の攻撃力が弱っている免疫環境を有しており、予後も不良であることがわかった。同様の評価を腎がん転移巣と、非淡明細胞型腎がんで行い、新規分類の再現性を確認した。
さらに、公開された公共データベースを用いた検討により、他がん種も今回の新規分類で分類可能なことが明らかになった。最後に研究グループは、個別の症例をLAG3、TIM-3、TIGIT優位群へ分類する臨床応用可能なワークフローを作成。このワークフローが実装可能であることを別の淡明細胞型腎がん組織を用いて確認した。
他がん種への応用にも期待
LAG-3、TIM-3、TIGITを標的とした次世代免疫チェックポイント阻害剤の開発は最終段階に入っている。抗LAG-3抗体と抗PD-1抗体の併用療法の皮膚悪性黒色腫を対象とした欧米における臨床試験での有効性が本年の米国臨床腫瘍学会で報告されるなど、近い将来日本でも上市されることが予想される。
今回、研究グループはLAG-3、TIM-3、TIGITを標的とした新規薬剤の治療候補症例を明らかにした。同研究が発展し、次世代免疫チェックポイント阻害剤の効果予測が可能となれば、新規薬剤を有効な患者へ届けることが可能になり、増大する医療費の抑制にも寄与することが期待される。また、がん免疫逃避機構は複数のがん種で共通していることが多く、免疫チェックポイント阻害剤はがん種横断的に有効性を示すことが特徴だ。研究グループは日本人のがん死亡数上位を占める肺がん・大腸がん・胃がんや皮膚悪性黒色腫を含む14のがん種も今回作成した新規分類で分類可能なことを示しており、同研究が発展すれば新規分類が他がん種でも応用可能となることが期待される。
▼関連リンク
・慶應義塾大学 プレスリリース



