一定のサイズを超える梗塞巣を呈した発症時刻不明脳梗への超急性期治療として
国立循環器病研究センターは12月14日、医師主導無作為割付試験であるTHAWS試験の第二弾の報告として、国内での独自用量(低用量)を用いた静注血栓溶解療法が一定のサイズを超える梗塞巣を呈した発症時刻不明脳梗塞患者への超急性期治療として有効であることを解明したと発表した。この研究は、同研究センターの豊田一則副院長が研究代表者を務める研究グループによるもの。研究成果は、「Stroke」電子版に掲載されている。
画像はリリースより
遺伝子組み換えによる組織型プラスミノゲン・アクティベータ(tPA)を用いた静注血栓溶解療法(以下、tPA静注療法)は、発症後4.5時間以内の治療開始が必要なため、睡眠中に発症して朝起床時に症状に気付く、言葉のコミュニケーションを取れなくなった状態を他者に発見されるなど、正確な発症時刻がわからない患者には使用できない。
このように、発症時刻不明脳梗塞患者の発症時刻を推測する手段の一つに、頭部MRIの拡散強調画像(DWI)とFLAIR画像での早期虚血所見の写り方の差、いわゆる「DWI-FLAIRミスマッチ(あるいはFLAIR陰性)」所見を用いる方法がある。DWIでは発症後30分程度で早期虚血所見を同定でき、FLAIR画像では同定までに約4~5時間を要するため、同定までの時間差を用いておおよその発症時刻を推測する。
研究グループは、THAWS試験を含めた国内外の大型臨床試験を統合解析した結果から、発症時刻不明脳梗塞患者をDWI-FLAIRミスマッチ所見などを用いて適切に試験に登録した場合に、tPA静注療法を有効かつ安全に使用できることを明らかにしている。また、国循が作成事務局を務めた2019年のtPA静注療法の指針改訂では、一足先にこのような治療法を推奨している。
国内独自0.6mg/kgのtPA静注療法、治療90日後の患者自立度評価のTHAWS試験
THAWS(THrombolysis for Acute Wake-up and unclear-onset Strokes with alteplase at 0.6 mg/kg)試験は、日本医療研究開発機構(AMED)の研究助成を受けて、国循を中心に国内多施設共同で行われ、主解析論文はStroke誌に掲載されている。DWI-FLAIRミスマッチ所見を有する発症時刻不明脳梗塞患者131人を、国内独自の低用量である0.6mg/kgのtPA静注療法群と標準内科治療群に無作為に割り付けて、治療90日後の患者自立度を修正ランキン尺度(「0(症状なし)」から「6(死亡)」までの7段階の評価尺度)を用いて調べた。その結果、完全自立の状態とみなされる同尺度の0または1の割合について試験全体では群間差を示さず、国内用量を用いてこの治療を行うことに、科学的裏付けを得ることができなかった。
THAWS試験では、近年著しく普及したカテーテル治療としての機械的血栓回収療法を併用できないなどの対象条件のため、軽症の脳梗塞患者に登録が偏りがちだった。そのため、DWIでの早期虚血所見の大きさは中央値2.5mL(四分位値0.5-11.5mL)と相当に小さく、全体の17%が早期虚血所見を全く認めない状態だった。この結果、標準内科治療群においても約半数が90日後に完全自立するという良好な結果を示し、tPA静注療法群がさらなる転帰改善効果を示すにはハードルが高かったと考えられたという。
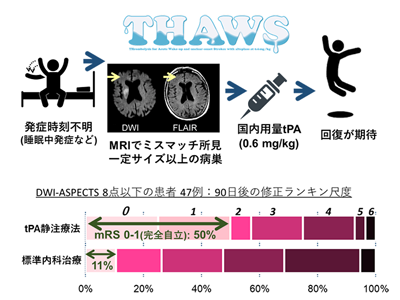
DWI-ASPECTS 8点以下の47例、90日後完全自立はtPA静注療法群で50%
今回実施したTHAWS試験のサブ解析では、早期虚血所見の大きさを定量的に測定、あるいは緊急の臨床現場で多用されるDWI-ASPECTS(11段階の肉眼的半定量尺度)で評価し、一定の早期虚血(梗塞)体積を超える患者のみを対象に患者自立度を比較し直した。
DWI-ASPECTSで大脳半球の複数領域に虚血が及ぶことを示す8点以下を呈した47例において、90日後に完全自立した患者はtPA静注療法群の50%、標準内科治療群の11%を占め、相対リスク4.75(95%信頼区間1.22-18.5)とtPA静注療法が有意に良好な結果を示した。
また、定量的測定で早期虚血体積が6.4mL(ROC解析から算出した閾値、直径23mmの球体に相当)を超える42例においても、tPA静注療法群(完全自立率38%)が標準内科治療群(6%)よりも転帰良好な傾向を示した(相対リスク6.15、95%信頼区間0.87-43.6)。
今回は少数例の検討、今後も臨床データの積み重ねが必要
今回の研究結果は、発症時刻不明脳梗塞患者に国内独自用量である0.6mg/kgのtPAを用いて治療を行うことについての科学的裏付けの一つと考えられる。しかし、今回は少数例の検討であり、また、主解析結果が有意差を示さなかった研究におけるサブ解析結果であることなどを考慮すれば、本治療の妥当性を示すために今後も臨床データの積み重ねが必要だという。
THAWS試験の研究グループでは現在、多施設共同観察研究THAWS2(UMIN-CTR臨床試験登録000040408)を行っており、その成果が待たれる。
▼関連リンク
・国立循環器病研究センター プレスリリース






