がん細胞の染色体異常の獲得過程は未知の領域
京都府立医科大学は8月11日、多発性骨髄腫において、有糸分裂チェックポイント分子であるBUB1の過剰発現が腫瘍細胞の染色体不安定性を亢進し、難治病態形成を促進していることを解明したと発表した。この研究は、同大大学院医学研究科血液内科学の黒田純也教授、分子診断治療センターの谷脇雅史特任教授の研究グループによるもの。研究成果は、「Cancers」に掲載されている。
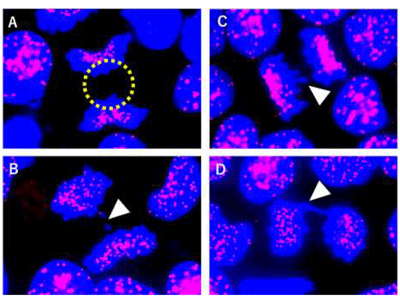
画像はリリースより
染色体異常や遺伝子の異常は、がんの発生とクローン性進化の根幹を担うイベントだ。がん細胞は1つの細胞の中に多くの染色体異常や遺伝子異常を同時に有し、その中にはがんの発生や悪化を直接的に促進するものと(ドライバー変異)、機能的な意義の乏しいもの(パッセンジャー変異)が混在する。そして、こうした多くの異常は、最初から全てがん細胞内に存在するわけではなく、最初に「創始者変異」と呼ばれる1つの異常が細胞に加わることでがん細胞の元になるクローンが発生し、これに加えて、細胞が増えたり生き残ったりするのに好都合な「ドライバー」として働く付加的・二次的な染色体異常や遺伝子異常が経時的・段階的に加わる。より悪性度の高いクローンが派生・増殖することで「がん」として成立し、さらに、より高悪性度で治療抵抗性のサブクローンが発生するという、がんの病態形成の過程が明らかになってきた。また、遺伝子変異が生じるメカニズムについても、多くのことが明らかになってきている。しかし、がん細胞の染色体異常の獲得過程は、未知の領域だ。
1つの染色体には、多くの重要な遺伝子が含まれているため、本来、染色体異常が生じた細胞は生き残ることも増えることも困難であり、細胞死に陥るはずだ。しかし、なぜ、がん細胞では染色体不安定性が高度であり染色体異常が生じるのか、なぜ染色体異常を獲得した細胞が生き残り、むしろ、高度悪性形質を有する細胞として増殖優位性を獲得しうるのかは、「がんのバイオロジー」を理解するための重要な課題として残されてきた。
有糸分裂チェックポイント分子BUB1が染色体分配エラーを許容、高度悪性化
多発性骨髄腫は血液腫瘍の中で2番目に多い疾患であり、高齢化社会において有病率は増加の一途にある。近年、治療薬の進歩は目覚ましいものがあるが、従来、極めて難治性であり、今も完治を得ることは容易ではなく、予後の改善をもたらす治療戦略の開発が求められている。骨髄腫では、染色体異常の獲得が初期の病態形成と悪性形質の高度化の両者において極めて重要だが、そのメカニズムには不明点が多く残されてきた。特に再発状態や、治療抵抗性獲得状態など難治状態では、治療初期には認めなかった高度の染色体異常が獲得されていることがしばしばであることから、クローン性進展によって病態悪化をもたらす染色体異常の獲得機序そのものを明確にし、その克服戦略が確立できれば、疾患悪化を抑制することが出来る可能性があるものと期待されてきた。
1つの細胞が2つの細胞に分裂することで細胞は増殖する。この時、新しい細胞には元の細胞と同じ量、同じ質の染色体が等しく分配される必要があるため、細胞分裂前には染色体は倍に増加し、これが正しく二等分されるために多くの細胞分裂制御分子が協調的に働くことが重要だ。BUB1は、本来、そのような過程で重要な役割を果たす有糸分裂チェックポイント分子だが、今回の研究では、多発性骨髄腫において、病勢進行とともにBUB1が正常の数倍以上に過剰発現し、むしろ、細胞分裂における染色体分配エラーを許容すること、ならびにそうした細胞のクローン性増殖を促進することが明らかになった。つまり、BUB1は適度の発現レベルであってこそ正しく機能することが可能であり、過剰発現すると、むしろ染色体不安定性の亢進によって、より高度悪性形質を有する腫瘍細胞の発生に一役買ってしまうことが判明したわけだ。
今回の成果について研究グループは、「多発性骨髄腫の多段階進展、クローン性進化の分子メカニズムの一端を明らかにした点で重要であり、BUB1、ならびに関連分子の制御が、疾患の高度悪性化を防ぐ突破口となる可能性を示したものと期待される」と、述べている。
▼関連リンク
・京都府立医科大学 お知らせ



