大腸特異的な抗菌物質Lypd8に注目、腸管バリア機構がGVHDに及ぼす影響について検討
北海道大学は7月2日、白血病などの血液悪性腫瘍の治療に用いられる同種造血幹細胞移植の合併症である腸管GVHD(移植片対宿主病)において、大腸杯細胞の障害が生じ、大腸杯細胞によって形成される粘液層のバリア機能が破綻することを、マウスモデルを利用して発見したと発表した。この研究は、同大大学院医学研究院の豊嶋崇徳教授、橋本大吾准教授らの研究グループによるもの。研究成果は、「Science Translational Medicine」に掲載されている。
画像はリリースより
同種造血幹細胞移植は白血病などの血液悪性腫瘍の根治的治療だが、感染症やGVHDはその代表的合併症であり、ときに致死的となる。近年、腸内細菌の乱れがGVHDや移植予後と関連することがさまざまなグループから報告されている。移植後に腸内細菌叢が乱れると有益な共生菌が減少し、有害な病原体の増殖が見られる。このような状況において、大腸杯細胞は糖タンパク質の一種であるムチンを分泌して粘液層を構成し、生体を防御する最後の砦としている。特に、腸内細菌の多くが存在する大腸では、粘液層は2層構造をとり、緻密な内層は腸内細菌に対する物理的バリアになるとともに、抗菌物質を内包することで、化学的バリアとしても機能している。
以前から腸管GVHDで杯細胞が減少することが知られていたが、その意義については不明だった。そこで研究グループは、マウスモデルとヒト臨床検体を用いて、大腸に特異的な抗菌物質である「Lypd8」に注目し、杯細胞が形成する粘液層による腸管バリア機構が腸管GVHD病態生理に及ぼす影響について検討を行った。
大腸粘液層がLypd8と協働して腸内細菌の侵入を防ぎ、GVHDの重症化を抑制
まず、マウスに骨髄移植を行い、同種移植後の大腸杯細胞数の変化、粘液層の形状変化、腸上皮への細菌の侵入について検討した。続いて、杯細胞増殖因子であるIL-25を骨髄移植前のマウスに投与して、杯細胞を保護した場合のGVHDに及ぼす影響について検討した。さらに、抗菌物質であるLypd8を欠損するノックアウトマウスにおいても同様の検討を行い、粘液層と抗菌物質との相互作用がGVHDに及ぼす影響について検討を行った。最後に、北海道大学病院で行った同種造血幹細胞移植を受けた患者から得られた大腸の生検検体を用いて、杯細胞の多寡とGVHDの有無や臨床経過との関係性について検討した。
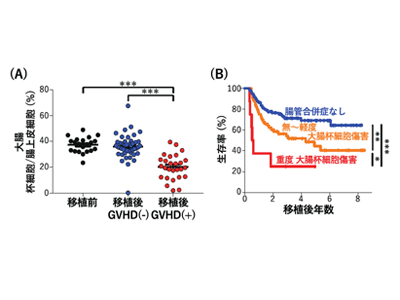
その結果、腸管GVHDでは大腸杯細胞が大きく減少していた。大腸杯細胞が傷害されることで、正常な粘液の2層構造は破綻し、腸上皮下への細菌浸潤が生じて、GVHDをさらに悪化させることが明らかになった。一方、IL-25を投与して杯細胞を保護することで、腸管GVHDが軽減されることも判明した。Lypd8は杯細胞とは異なる腸上皮細胞から分泌される大腸特異的な抗菌物質で、細菌の運動性を阻害して細菌の生体内への侵入を防ぐ。腸管GVHDではLypd8の産生自体は正常だったが、粘液層の破綻によってLypd8を高濃度に保持することが困難になることがわかった。IL-25を用いた杯細胞保護によるGVHD軽減効果は、Lypd8ノックアウトマウスでは認められなかったことから、杯細胞が形成する大腸粘液層はLypd8と協働して、腸内細菌の侵入を防ぎ、GVHDの重症化を抑制していることがわかった。
杯細胞の傷害度は移植予後と相関、重度の傷害を受けた群では死亡率高く
同種造血幹細胞の移植後には、さまざまな腸管合併症をきたすが、患者検体を用いた検討では腸管GVHDで特異的に大腸杯細胞が減少していた。また、その減少度は腸管GVHDの重症度に比例し、治療によるGVHDの改善に伴って、杯細胞も回復していた。さらに、杯細胞の傷害度は移植予後と相関し、重度の傷害を受けた群ではより死亡率が高いことがわった。
今回の研究で、大腸杯細胞や抗菌物質Lypd8のGVHD病態形成における意義が解明されたことで、これらが新たなGVHD予防・治療のターゲットとなり得ることがわかった。研究グループは、「臨床においては、大腸杯細胞が腸管GVHDの診断・治療モニター・予後予測の新たなバイオマーカーとなることが期待される」と、述べている。
▼関連リンク
・北海道大学 プレスリリース






