主流のハイドロゲルは移植後に体内に分散、完全に取り出すことに難
東京大学は6月17日、マウスの腹腔に直径の異なるハイドロゲルファイバーを移植する研究から、直径が「ミリメートルスケール」のファイバーは、「マイクロメートルスケール」のファイバーと比べて、異物として認識されにくいことを発見したと発表した。これは、同大生産技術研究所/大学院情報理工学系研究科知能機械情報学専攻の竹内昌治教授、生産技術研究所の興津輝特任教授、渡邉貴一特任研究員(研究当時)らの研究グループによるもの。研究成果は、「Biomaterials」のオンライン版に掲載されている。
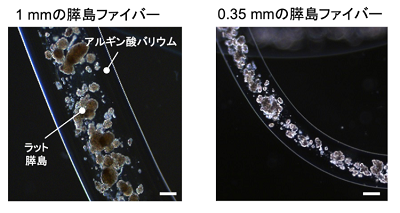
画像はリリースより
1型糖尿病の治療法として、ドナーから得た膵島をハイドロゲルで覆い、それをレシピエントに移植することによって、糖尿病患者の血糖値を正常化する細胞療法が世界中で盛んに研究されている。特に近年、iPS細胞から膵島の細胞を作製する方法が進展し、膵臓移植のドナー不足解消の機運が高まり、さまざまな移植技術が開発されている。
ドナー細胞の機能をレシピエントの体内で長期間維持するためには、細胞を保護するハイドロゲルが細胞の養分や老廃物を通過し、免疫系細胞を通過しない半透膜性を示すだけでなく、ハイドロゲル自体が激しい異物反応を受けないことが重要だ。これまでの研究では、細胞を保護するハイドロゲルの形状として、ビーズ形状が主流だった。しかし、ビーズ形状のハイドロゲルは、移植後に体内に分散するため、移植した細胞に機能障害が起こっても完全に取り出すことは困難で、レシピエントの安全性に問題があった。そのため、生体内での異物反応を受けにくく、取り出し可能なハイドロゲル移植材料の開発が望まれていた。
糖尿病マウスにミリスケールのファイバー移植で、移植後100日以上の血糖値正常化を達成、取り出しも成功
研究グループは今回、移植材料として、ファイバーの中心部(コア)をチューブ状の外殻部(シェル)が覆っている「コアシェル型」という構造を持つファイバーを、マイクロ流体デバイスを用いて作製した。中心部であるコアには、グルコースの濃度に応答してインスリンを分泌するラット膵島と、細胞外基質(Extracellular matrix)の成分であるコラーゲンを混ぜたものを使用した。外殻部であるシェルには、「アルギン酸バリウムハイドロゲル」という、機械的強度が高く、細胞の養分や老廃物が通過できる材料を使用した。
マイクロ流路を用いて、直径がマイクロスケールのファイバーとミリスケールのファイバーを作製し、それぞれ免疫系を持つ糖尿病マウスの腹腔に移植。その結果、マイクロスケールのファイバーの場合、移植後10日以内に体内での激しい異物反応によって血糖値を正常化する機能が失われた。一方、ミリスケールのファイバーの場合、異物反応を抑制することによって、移植後100日以上という長期での血糖値正常化を達成した。さらに、体内に分散しないファイバー状の形を生かして、必要に応じて体内からファイバーを取り出すことにも成功した。
「このハイドロゲルファイバーは、膵島に限らず、神経細胞や肝細胞、iPS細胞から作った細胞などをレシピエントに移植する際の保護材料として、さまざまな移植治療への応用展開が期待される」と、研究グループは述べている。
▼関連リンク
・東京大学生産技術研究所 ニュース



