開発した新規培養法により、高品質なキラーT細胞が効率よく誘導可能に
京都大学は4月15日、患者のがん組織を移植したマウスモデルを用いて、ヒトiPS細胞から再生した汎用性の高いキラーT細胞が、固形がんの一種である腎がんに効果があることを示したと発表した。これは、同大ウイルス・再生医科学研究所の河本宏教授らの研究グループが、同大医学部附属病院の嘉島相輝助教(現・秋田大学医学部附属病院助教)らと共同で行ったもの。研究成果は、「iScience」のオンライン版に掲載されている。
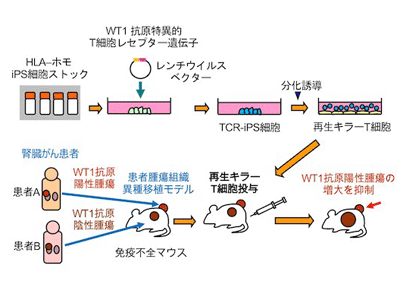
画像はリリースより
抗PD-1抗体や抗CTLA-4抗体などの免疫チェックポイント阻害剤が一部のがんに奏効するということは、がん患者の体の中に、がん細胞を殺す力を有するキラーT細胞が存在していることを示している。実際に、T細胞を患者から採取して、遺伝子を操作した上で患者に戻す方法(養子免疫療法)が、がんの治療に有効であることが示されてきた。しかし、そのような自家移植で行う治療法は「コストがかかる」「時間がかかる」「患者のT細胞の質に依存するので投与するT細胞の品質が不安定」などの問題があった。
研究グループは、この問題を解析するために、iPS細胞技術を用いることを考えた。T細胞はT細胞レセプターを細胞表面に出しており、このレセプターを使って標的になる分子を認識する。このT細胞レセプターは、「遺伝子再構成」と呼ばれる仕組みによって作り出された遺伝子から作られる。がん細胞に特有の抗原(がん抗原)を認識できるT細胞レセプターを有するT細胞からiPS細胞を作製すると、そのiPS細胞には再構成されたT細胞レセプター遺伝子の構造が受け継がれる。そのiPS細胞からT細胞を再生すれば、がん抗原を認識できるT細胞だけ、新鮮で元気なT細胞を必要なだけ作ることができる。
研究グループは、この発想に基づき、2013年に世界で初めてがん抗原に反応するヒトのキラーT細胞の再生に成功し、論文発表した。この論文では、悪性黒色腫に特有のがん抗原であるMART-1抗原を標的にした。しかし、この時点での技術では、再生したキラーT細胞の品質はあまり良くなかった。この問題を解決するため、2016年に培養法の改良を実施。新しい培養法により、高品質なキラーT細胞が効率よく誘導できることがわかった。さらにこの方法を、WT1抗原という急性骨髄性白血病で高発現しているがん抗原に応用。再生キラーT細胞は、WT1抗原を有している白血病細胞株を効率よく殺傷した。また、ヒト白血病細胞を免疫不全マウスに注入して作製する白血病モデルを用いた実験で、再生キラーT細胞を投与することにより、治療効果がみられた。
他家移植用iPS細胞に臨床試験済みのTCR遺伝子を導入、WT1認識キラーT細胞を再生
今回の研究は、iPS細胞に外来のTCR遺伝子を導入する(TCR-iPS細胞法)という、これまでとは異なる方法で行った。TCR-iPS細胞法は2014年に出願し、欧州で特許査定を受けたもの。この方法を他家移植の系で使えば、「すでに効果や安全性が確かめられたTCR遺伝子を用いることができる」「他家移植用のiPS細胞を用いることができる」ことから、再生T細胞を用いる戦略の汎用性が格段に高くなると推察された。
他家移植用のiPS細胞としては、京都大学iPS細胞研究所が作製しているHLAハプロタイプホモ(HLAホモ)のiPS細胞ストックを用いた。HLAホモiPS細胞から再生した組織や細胞は、同じHLAハプロタイプをヘテロで有する患者に移植した時に、免疫拒絶が起こりにくいことが期待される。また、現在頻度の高い順に上位4種類の株が入手可能で、この4種類で日本人の35%をカバーできるという。
研究グループはまず、iPS細胞研究所から入手した最も頻度の高いHLAホモiPS細胞株に、レンチウイルスを用いてWT1-TCR遺伝子(TAK1)を導入(WT1-TCR-iPS細胞)。WT1-TCR遺伝子は愛媛大学の安川正貴教授らが樹立した、TAK1というキラーT細胞クローンから単離されたTCRで、このTCRを用いたTCR遺伝子導入療法の臨床試験が急性白血病あるいは骨髄異形成症候群に対して行われ、一定の治療効果が報告されている。
このWT1-TCR-iPS細胞を、OP9細胞、引き続いてOP9/DLL1細胞と共培養すると、35日目にはCD4CD8共陽性細胞(DP細胞)が生成した。磁気ビーズを用いてDP細胞を単離し、WT1ペプチドを負荷した抗原提示細胞(Bリンパ芽球様細胞株)を用いて刺激を入れると、キラーT細胞が生成した。生成したキラーT細胞は、CD8αβヘテロダイマーを発現するCD8T細胞で、ほぼ全てがWT1テトラマーに反応するTCRを発現していた。
固形がんモデルとして腎がんへの効果を検証、腫瘍増大抑制を確認
今回は、再生CTLを用いた戦略をより一般化するために、固形がんを対象とした開発研究を行った。治療モデルとしては、WT1抗原を発現している腎がんを標的として用いた。腎がんは、悪性黒色腫や非小細胞性肺がんと同様、免疫原性の高いがんとして知られている。固形がんに対象を拡げるに際し、最初の標的疾患として適切であると考えたという。
臨床試験に近い条件にするために、細胞株を用いるのではなく、患者腫瘍組織移植モデル(Patient-derived xenograft model:PDX)を用いた。PDXモデルでは患者がん組織が有している不均質性や階層性が維持されているため、元のがん組織の性質に近いと考えられている。この腎がんPDXモデルを用いて、再生キラーT細胞の治療効果を測定した。WT1陽性腫瘍組織を免疫不全マウス(NOGマウス)の背中の右側、WT1陰性腫瘍組織を左側に皮下移植した。移植1週間後から、再生CTL107細胞/回を週3回、計12回腹腔内投与した。その結果、治癒には至らなかったが、腫瘍の増大を抑制する効果が認められた。この結果により、固形がんに対するTCR-iPS細胞を用いた研究グループの戦略は、臨床応用に向けて大きく前進したと言える。
今回、T細胞の材料として用られたのはHLAを出しているiPS細胞で、型が合う人は6人に1人しかいない。しかし、将来的には誰にでも使えるiPS細胞が作られると考えられる。そのようなiPS細胞に、今回のような方法でTCR遺伝子を導入し、そのiPS細胞から再生T細胞を作製すれば、誰にでも使えるがん抗原特異的なT細胞を作製できるという。一方、iPS細胞自体は誰にでも投与することができても、T細胞レセプターは、特定のHLAを持っている人にしか使えない。今回使用したWT1抗原特異的T細胞レセプターは、日本人の6割に使えるもの。研究グループは、「今後、いろいろなT細胞レセプターを用いれば、幅広く多くの人に使えるようになると期待できる。日本は抗体製剤の開発競争では世界に大きく遅れをとったが、われわれが進めている再生T細胞療法は、現時点では世界をリードしている。今後も日本発のこの技術を発展させ、優位性を保ちたいと考えている」と、述べている。
▼関連リンク
・京都大学 研究成果



