既存治療薬の効果は限定的、早期の病態解明が課題
慶應義塾大学は11月20日、筋萎縮性側索硬化症(ALS)の患者から採取した脳脊髄液に、極めて細胞毒性の高いタンパク質「SOD1」が含まれていることを世界で初めて発見した。これは、同大理工学部の古川良明准教授、徳田栄一助教(研究当時。現・日本大学薬学部専任講師)と、独立行政法人国立病院機構まつもと医療センター脳神経内科の大原慎司副院長(現・飯田病院神経内科)、岐阜薬科大学薬物治療学の保住功教授、兵庫医科大学生化学講座の藤原範子教授らとの共同研究によるもの。研究成果は国際科学誌「Molecular Neurodegeneration」に掲載されている。
画像はリリースより
ALSの日本国内患者は約1万人と報告されている。発症年齢や罹病期間などは患者によって異なるが、筋力低下・筋萎縮・まひなどの症状とともに、発症後3〜5年ほどで呼吸困難となるため、人工呼吸器による補助が必要になる。認可されているALS治療薬はリルゾールとエダラボンという2剤しかなく、その効果も限定的であることから、ALSの病理解明と根本的な治療法の早期開発が求められている。
孤発性ALSでもミスフォールドしたSOD1があるか患者の脳脊髄液で検討
遺伝性ALSの研究により、病因性の変異が最初に同定されたSOD1(銅・亜鉛スーパーオキサイドディスムターゼ)遺伝子に関する研究は、非常に盛んだ。遺伝子産物である変異型SOD1タンパク質が、異常な分子構造を形成して(ミスフォールドして)、運動ニューロン内に蓄積するといった特徴も知られている。つまり、遺伝子変異に伴うアミノ酸置換によってSOD1タンパク質の天然構造が不安定になり、ミスフォールドしたSOD1タンパク質が運動ニューロンに対して毒性を発揮することで、ALSが発症すると推測されている。ただし、SOD1遺伝子に変異が認められるALSは全症例の約1割に過ぎない。
つまり、多くの患者ではSOD1は野生型である。孤発性ALSの患者に、ミスフォールドした野生型SOD1が検出されるのかは見解が明確にわかれている。従来の研究では、ALSの主要な病変部位である「脊髄」において、ミスフォールドしたSOD1 タンパク質の有無が論じられてきたが、その存在についてはコンセンサスが得られていない。そこで研究グループは、脳や脊髄における変化をより鋭敏に反映すると考えられる「脳脊髄液」(CSF)に着目し、孤発性ALSやその他の患者から採取したCSFに含まれるSOD1がミスフォールドしているのかを検討した。
ALSを含む神経変性疾患患者でミスフォールドしたSOD1を確認
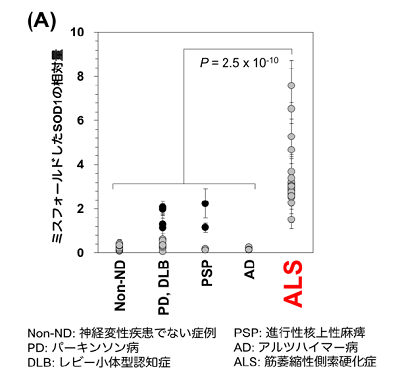
研究グループはまず、サンドウィッチELISAという手法を用いて、CSFにおけるミスフォールド型SOD1の極微量検出を実現した。その上で、21人のALS患者のCSFを調べたところ、すべての患者からミスフォールドしたSOD1を検出した。また、パーキンソン病や進行性核上性まひといった他の神経変性疾患の患者の一部からもミスフォールドしたSOD1を検出したが、神経変性疾患ではない患者のCSFからは全く検出されなかった。
次に、ミスフォールドしたSOD1が神経細胞の変性に関与しうるのかを検討するため、その毒性について培養細胞を用いた評価を行った。ALS患者から採取したCSFを運動ニューロン様の培養細胞であるNSC-34に添加すると、細胞の生存率がおよそ40%に低下。ミスフォールドしたSOD1を免疫沈降法によってCSFから除去すると、生存率は80%まで回復した。ウェスタンブロット法を用いたCSFに含まれるミスフォールド型SOD1の濃度はpmol/Lのレベルと概算で確認され、その細胞毒性は極めて高いことが判明した。
今回の研究で、孤発性ALS患者のCSFにはミスフォールドした野生型SOD1タンパク質が含まれており、それらは極めて高い細胞毒性を発揮することを初めて明らかにした。他の神経変性疾患の患者の一部からもミスフォールドしたSOD1が検出されたことから、ミスフォールドしたSOD1はALS以外の疾患を理解する上でも重要な物質であることが示唆される。しかし、ミスフォールドしたSOD1がALSの発症や症状の悪化に対して直接に関与しているのか、あるいは、病気の結果として生じる産物にすぎないのか、さらなる検証が必要だ。また、ミスフォールドしたSOD1が神経細胞に対して毒性を発揮するメカニズムを明らかにできれば、神経難病の最たる例であるALSの治療薬開発に新たな展開が期待される。
▼関連リンク
・慶應義塾大学 プレスリリース



