神経堤細胞の分化制御について、抑制メカニズムの解明へ
京都大学は10月21日、心臓の中に軟骨ができないようにする仕組みが備わっていることを発見したと発表した。この研究は、同大ウイルス・再生医科学研究所の荒井宏行研究員、瀬原淳子名誉教授と、同大iPS細胞研究所、理化学研究所、広島大学、岐阜大学、英・Newcastle大学らとの共同研究グループによるもの。研究成果は、国際学術誌「Cell Reports」にオンライン掲載された。
画像はリリースより
動物の体が形作られる過程では、細胞は適切な場所で適切な機能を持つ細胞になるため、制御を受ける必要がある。さまざまな細胞へ変化(分化)する能力をもつ「神経堤細胞」の分化制御について、どのように誘導されるのかについては多くの研究がされているが、どのように抑制されるのかについては不明な点が多く残されている。
FOPなど異常な軟骨形成・分化の病態を示す病気の治療へ応用
研究グループはまず、Adam19欠損マウスの心臓神経堤細胞が異所性軟骨を形成し、マイクロアレイによる遺伝子発現解析を行った。その結果、Adam19欠損型では軟骨細胞分化に重要な役割を果たすSox9遺伝子の発現が高くなっていることが判明した。次に、このSox9と異所性軟骨形成の関係性について調べたところ、Adam19欠損マウスの神経堤細胞においてSox9の発現を減少させると、異所性軟骨の形成が消失した。反対に、神経堤細胞でSox9を過剰発現させたマウスは、Adam19欠損マウスと同様に、心臓に異所性軟骨を形成した。これらの結果から、Adam19欠損による異所性軟骨形成は、Sox9遺伝子の発現上昇に起因することが示唆された。
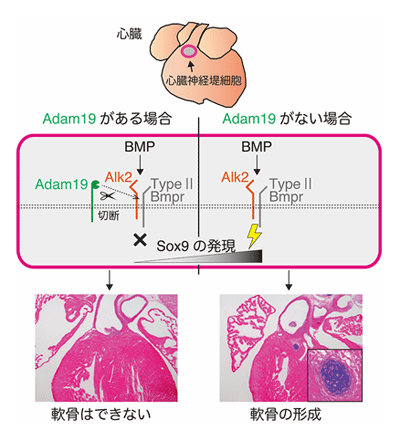
これまでAdam19は、1回膜貫通型のメタロプロテアーゼで、細胞膜に存在する膜型増殖因子等のタンパク質を切断すると考えられてきたが、その生理的基質の実体は不明だった。BMPシグナルがSox9の発現を正に制御すること、異所性軟骨形成が神経堤細胞特異的Adam19欠損マウスでも再現されたことから、Adam19が、心臓神経堤細胞でBMP受容体を切断し、BMPシグナル伝達を抑制するという仮説を立て検証した。培養細胞実験から、Adam19がBMP受容体の1つであるAlk2(Acvr1)を選択的に切断することが明らかになった。この結果を生体マウスで検証するため、Alk2/Alk3のインヒビターであるLDN−193189をAdam19欠損マウスに投与すると、異所性軟骨の形成が阻害されたことから、同仮説が裏付けられた。
これらの結果から、心臓神経堤細胞で発現するAdam19が、Alk2の切断を介したBMP-Sox9のシグナル経路の抑制により、軟骨細胞分化を積極的に抑制するという、神経堤細胞分化の新たなメカニズムが示唆された。
研究グループは、「今回の研究成果は、体を形作る仕組みの1つとして、「心臓神経堤細胞自体に軟骨形成 ・分化を抑制するシステム」が備わっていることを示唆している。また、この抑制因子の投与や抑制システムを活性化させることで、異常な軟骨形成・分化の病態を示す病気の治療に応用できる可能性が生まれたと言える」と、述べている。
▼関連リンク
・京都大学 研究成果






