細胞・組織障害が非常に少ない低侵襲治療としてさまざまな分野で注目されるLIPUS
東北大学は7月20日、低出力パルス波超音波(low-intensity pulsed ultrasound:LIPUS)が、心臓の収縮力(左室駆出率)の保たれた心不全(heart failure with preserved ejection fraction:HFpEF)のモデルマウスにおいて有効かつ安全であることを示し、その詳細な作用機序を明らかにしたと発表した。この研究は、同大大学院医学系研究科循環器内科学分野の下川宏明客員教授、進藤智彦助教、門間雄斗医師らの研究グループによるもの。研究成果は、欧州心臓病学会学会誌「Cardiovascular Research」にオンライン掲載されている。
画像はリリースより
心不全は、先進諸国における主要な死因となっており、その患者数は増加している。現時点において、全世界で患者数は約2,600万人と想定されており、「心不全パンデミック」と称されている。日本でも、心不全患者数は急激に増加しており、2030年には約150万人に達すると予想されている。
従来、心不全の原因は、左心室の収縮力が低下し(左室駆出率が50%未満)、左心室が拡大した収縮不全が主な原因と考えられていた。しかし、近年、心不全患者の中には、収縮力が保たれているにもかかわらず、左心室が硬くて広がりにくいために、心不全症状を呈する拡張不全というタイプの心不全があることがわかってきた。心臓へ血液を戻す力が弱くなっているため、うっ血が起こり、むくみや労作時の息切れなどの症状が起こる特徴がある。このタイプの心不全を、HFpEFと呼ぶ。その患者数は心不全患者全体の半数以上を占め、世界的にも急増していることから、世界的な問題となっている。
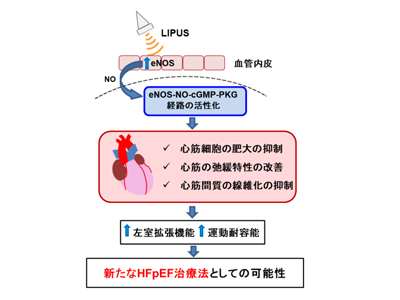
HFpEFの病態については未解明な部分が多いが、近年では血管内皮障害、特に、内皮型一酸化窒素合成酵素(endothelial nitric oxide synthase:eNOS)の機能障害がその主な病態の一つではないかと考えられている。高血圧や糖尿病、脂質異常症といった併存症により、全身性に酸化ストレスや炎症が惹起された結果、血管内皮の障害、それに引き続くeNOSが関与するシグナル伝達経路(eNOS-NO-cGMP-PKG経路)の障害が起こり、左室の拡張障害が生じ、HFpEFの発症につながるというもの。これまでの心不全治療薬の開発は、収縮不全タイプの心不全を治療標的としており、その結果、β遮断薬、ACE阻害薬など有効な薬剤が数多く開発されてきたが、HFpEFに関しては有効な薬剤の開発には至っていないのが現状だ。このような中、近年、LIPUSは、細胞・組織障害が非常に少ない低侵襲治療としてさまざまな分野で注目されている。
LIPUS治療を受けたモデルマウス、左室拡張能の改善や心不全バイオマーカーBNPの低下
これまでに、下川客員教授らの研究グループは、狭心症や心筋梗塞などの虚血性心疾患において、LIPUSが血管内皮細胞の細胞膜の窪み構造(カベオラ)を伸展させることで、細胞膜表面の機械刺激受容体を刺激し、eNOSの発現および血管新生を誘導することを明らかした。
そこで、今回、研究グループは、LIPUS治療がHFpEFの拡張障害を改善し有効な治療法になるのではないかと着想し、HFpEFモデル動物(マウス)に対する有効性・安全性を検討する目的で一連の実験を実施。その結果、LIPUS治療を受けた動物では、左室拡張能の改善、心不全のバイオマーカーであるBNPの低下、運動耐容能の改善、心筋の肥大・線維化の低減、心筋組織レベルでの弛緩特性の改善が認められ、その機序としてeNOS-NO-cGMP-PKG経路の活性化が関与していることを見出した。
研究グループは、同研究について、HFpEFモデルマウスに対するLIPUS治療が効果的かつ安全であることを示す世界で最初の報告だとし、いまだ有効な治療法が確立されていないHFpEF患者に対して、LIPUS治療が新たな治療戦略になる可能性が示された、と述べている。
▼関連リンク
・東北大学 プレスリリース






