「第5のがん治療法」として注目のBNCTは再発性・多発性にも有効
東京工業大学は1月23日、液体のりの主成分である「ポリビニルアルコール」(以下、PVA)をホウ素化合物「ボロノフェニルアラニン」(以下、BPA)に加えるだけで、中性子捕捉療法(Boron Neutron Capture Therapy:BNCT)の治療効果を大幅に向上できることを発見し、マウスの皮下腫瘍をほぼ消失させることに成功したと発表した。これは同大科学技術創成研究院化学生命科学研究所の野本貴大助教と西山伸宏教授(川崎市産業振興財団ナノ医療イノベーションセンター主幹研究員兼任)の研究グループによるもの。研究成果は、「Science Advances」に掲載されている。
画像はリリースより
BNCTは、ホウ素と熱中性子の反応を利用して、正常細胞にあまり損傷を与えず、腫瘍細胞のみを選択的に破壊する放射線療法。従来の方法では治療することが困難な再発性のがん、多発性のがんに対しても有効であるため、第4のがん治療法と呼ばれる免疫療法に続く、「第5のがん治療法」として大きな期待を集めている。BNCTでは、いかにホウ素をがん腫瘍に選択的に集積させることができるかが重要となる。
BPAの臨床試験で奏効率71.4%、一方、がん腫瘍での滞留性に課題
BPAは、LAT1というがん細胞上に多く発現しているアミノ酸トランスポーターを介して細胞に取り込まれる性質があるため、選択的にがんに集積することができる化合物である。現在、BPAの臨床試験はステラファーマ株式会社が行っており、P2試験において、再発頭頸部がんに対しBNCT施行90日後の奏効率が71.4%という治療効果が得られている。しかし、BPAは長期的にはがん細胞に滞留することができないケースもあり、滞留性を長期化できれば、BNCTの治療効果をさらに向上できると考えられてきた。
BPAががん細胞に長期的に留まることができない原因の一つとして、LAT1の交換輸送メカニズムが関連していると考えられている。LAT1は細胞外のBPAを取り込む際に細胞内のアミノ酸を排出するが、細胞外のアミノ酸を取り込む際に細胞内のBPAを排出することもある。その結果、細胞外のBPA濃度が低下すると細胞内のBPAが流出してしまう現象が起きる。
「スライムの化学」を利用しPVAに結合したBPA作製、がん細胞への滞留長期化に成功
このような細胞外へのBPAの流出を抑えるために、液体のりとホウ砂から作られるスライムと同様の化学反応を利用した方法を開発した。液体のりの主成分であるPVAは、生体適合性の高い材料として古くから研究されてきた物質であり、さまざまな医薬品の添加物としても使用されている。PVAは多くのジオール基を持っており、このジオール基はホウ酸やボロン酸と呼ばれる構造と水中でボロン酸エステル結合を形成することができる。研究グループはこの化学を利用してBPAをPVAに結合させたところ、PVAに結合したBPA(PVA-BPA)はLAT1介在型エンドサイトーシスという経路で細胞に取り込まれるようになり、従来のBPAが細胞質に蓄積するのに対し、PVA-BPAはエンドソーム・リソソームに局在するようになった。その結果、がん細胞に取り込まれるホウ素量が約3倍に向上し、細胞内で高いホウ素濃度を長期的に維持することが可能となった。
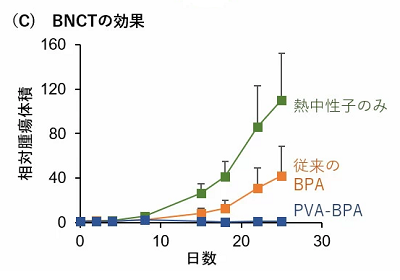
さらに、京都大学研究用原子炉でマウスの皮下腫瘍モデルを用いて、がんへの集積性を評価したところ、従来のBPAと同等以上の集積性を示した。従来のBPAは徐々に腫瘍内の集積量を低下させた一方で、PVA-BPAはその高いホウ素濃度を長期的に維持することができた。そして、熱中性子を照射すると、PVA-BPAは強力な抗腫瘍効果を示し、ほぼ根治に近い結果を得ることができた。
PVA-BPAはスライムを作るように、水中でPVAとBPAを混ぜるだけで簡単に合成することが可能である。製造が容易である上に治療効果も非常に優れていることから本研究成果は極めて実用性が高いと考えられる。「今後、ステラファーマ社の協力を得てさらなる研究を行い、安全性を精査しながら臨床応用への可能性を検討していく予定である」と、研究グループは述べている。
▼関連リンク
・東京工業大学 東工大ニュース



