「軸索」の異常がALSの病態解明の糸口として注目
東北大学は7月2日、筋萎縮性側索硬化症(ALS)患者由来のiPS細胞を用いてALS運動ニューロンの新たな病態を発見したと発表した。この研究は、東北メディカル・メガバンク機構の秋山徹也助教、東北大学大学院医学系研究科神経内科学分野の鈴木直輝助教、割田仁院内講師、青木正志教授、慶應義塾大学医学部生理学教室の岡野栄之教授らの研究グループによるもの。研究成果は、オープンアクセス学術誌「EBioMedicine」に掲載されている。
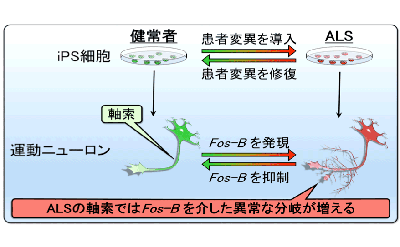
画像はリリースより
国の指定難病となっているALSは、運動ニューロンの障害を特徴とする神経変性疾患。ALSのうち約10%が家族性(遺伝性)で、20以上の原因遺伝子が発見されているが、病態は未解明で根本的治療法はない。ALSでは、神経細胞に特徴的な構造である「軸索」が、ALSの運動ニューロン変性の初期に障害されるため、軸索異常が病態解明の糸口として注目されてきたが、実験に十分な量の軸索を集めることが難しく研究が困難だった。近年の人工多能性幹細胞(iPS細胞)の発見は、ALS患者から病変組織の検体を取ることが困難であった神経変性疾患研究のブレークスルーとなり、病態解明のための研究手法として確立されつつある。
軸索形態異常の原因としてFos-B遺伝子を同定
今回、研究グループは、家族性ALSの原因遺伝子のうち、日本人で2番目に多いfused in sarcoma(FUS)遺伝子に注目。FUSに変異を持つ家族性ALS患者からiPS細胞を樹立した。さらに、健常者由来のiPS細胞やALS患者由来のiPS細胞のFUS遺伝子をゲノム編集技術により組み換え、人為的な健常株とALS株を作成した。それらのiPS細胞から運動ニューロンを誘導して細胞の形を確認した結果、FUS遺伝子に変異がある運動ニューロンの軸索では分岐が増えるという現象を見出した)。同様の軸索形態の変化は、ほかのALS原因遺伝子であるSOD1遺伝子やTARDBP遺伝子の変異によっても生じることを明らかにし、ALSに共通する表現型である可能性を示した。
さらに、軸索のみを回収できるNerve organoid deviceと呼ばれるマイクロ流体デバイスと、RNAシーケンスを組み合わせて軸索のRNAを分析する手法を確立し、軸索形態異常に関連する因子としてFos-Bを同定。ALS株ではFos-Bの発現が増加しており、Fos-Bの抑制により、FUS変異を有する運動ニューロン軸索の形態は改善できたことから、Fos-Bが治療標的となる可能性を見出した。また、Fos-Bを人工的に発現させることで、健常なiPS細胞由来の運動ニューロンだけでなく、小型モデル魚類ゼブラフィッシュの運動ニューロン軸索も異常に分岐することを確認し、生体内におけるFos-Bの機能の重要性も示した。
今回の研究成果はALSの運動ニューロンの軸索形態の異常という新たな表現型を明示しただけでなく、その表現型に関連する因子Fos-Bを世界で初めて明らかにした重要な報告。また、従来検討が困難であったが、今回可能となったヒトの運動ニューロンの軸索の解析法は、ALS以外の神経変性疾患へも応用可能な技術基盤となりえる。「軸索形態の変化は運動ニューロン変性より先におこるため、Fos-BはALSの早期治療標的として期待されるだけでなく、Fos-Bによる軸索形態変化への影響は神経発生・再生のメカニズムを解明する上でも重要と考えられる」と。研究グループは述べている。
▼関連リンク
・東北大学 プレスリリース






