急性リンパ芽球性白血病試験
フランスのバイオ製薬企業エリテックは、急性リンパ芽球性白血病(ALL)の第3相試験への患者組入れが完了したと発表した。ALLは悪性度の高い白血病。特に高齢患者と再発患者は、従来の治療薬に対する忍容性がない場合が多く、長期全生存率は10%から30%と非常に低いため、医療ニーズが高い。
今試験は、再発性又は難治性ALLの小児患者及び成人患者80例を対象とした多施設ランダム化対照臨床試験で、同社の主力製品「GRASPA(R)」を天然アスパラギナーゼと比較するもの。フランス・ベルギー・スペインで58施設が参加するという。
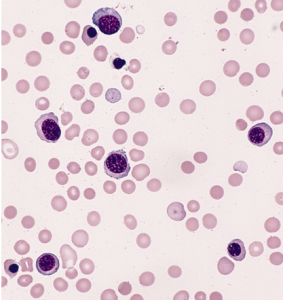
(画像はwikiメディアより引用)
試験の経緯
この試験は元々2009年に第2/3相試験として開始されたが、独立データ安全性モニタリング委員会(DSMB)が最初の患者60例のデータを検討した結果、第3相試験に移行し、治験実施計画書を変更せずに試験の続行を勧告した。
アスパラギナーゼは、その毒性プロファイルにより高齢者、虚弱患者における使用には制限がある。GRASPAは、酵素を赤血球内に封入して保護するため、従来の製剤よりも安全性が高く、臨床用途が広いという。
既に、再発性の小児及び成人患者における第1/2相試験と、新規にALLの診断を受けた55歳以上の患者における第2相試験を完了し、いずれの試験でも安全性プロファイルの改善と、良好な有効性を示すデータが得られているという。同社は、この製剤により、オンコロジー分野におけるニーズに応えることができることに大きな期待がもてると述べている。(堤朝子)
▼外部リンク
QLifePro プレス
https://www.qlifepro.com/press/




